Синонимы, аналоги
Статьи
Регистрационный номер:
ЛСР-009820/09
Торговое наименование:
Ксарелто®
Международное непатентованное наименование:
ривароксабан
Лекарственная форма:
таблетки покрытые пленочной оболочкой
Состав
1 таблетка покрытая пленочной оболочкой содержит:
действующее вещество: ривароксабан микронизированный — 10,00 мг;
вспомогательные вещества: целлюлоза микрокристаллическая — 40,00 мг, кроскармеллоза натрия — 3,00 мг, гипромеллоза 5 сР (Гидроксипропилметилцеллюлоза 2910) — 3,00 мг, лактозы моногидрат — 27,90 мг, магния стеарат — 0,60 мг, натрия лаурилсульфат — 0,50 мг; оболочка: краситель железа оксид красный — 0,015 мг, гипромеллоза 15 сР (Гидроксипропилметилцеллюлоза 2910) — 1,500 мг, макрогол 3350 (Полиэтиленгликоль (3350)) — 0,500 мг, титана диоксид — 0,485 мг.
Описание
Круглые двояковыпуклые таблетки розового цвета покрытые пленочной оболочкой; методом выдавливания нанесена гравировка: на одной стороне — треугольник с обозначением дозировки (10), на другой — фирменный байеровский крест.
Фармакотерапевтическая группа:
прямые ингибиторы фактора Ха
Код ATX:
B01AF01
Фармакологические свойства
Фармакодинамика
Механизм действия
Ривароксабан — высокоселективный прямой ингибитор фактора Ха, обладающий высокой биодоступностью при приеме внутрь.
Активация фактора Х с образованием фактора Ха через внутренний и внешний пути свертывания играет центральную роль в коагуляционном каскаде. Фактор Xa является компонентом формирующегося протромбиназного комплекса, действие которого приводит к превращению протромбина в тромбин. В результате эти реакции приводят к формированию фибринового тромба и активации тромбоцитов тромбином. Одна молекула фактора Xa катализирует образование более 1000 молекул тромбина, что получило название «тромбинового взрыва». Скорость реакции связанного в протромбиназе фактора Xa увеличивается в 300000 раз по сравнению с таковой свободного фактора Xa, что обеспечивает резкий скачок в уровне тромбина. Селективные ингибиторы фактора Xa могут остановить «тромбиновый взрыв». Таким образом, ривароксабан оказывает влияние на результаты некоторых специфических или общих лабораторных исследований, применяемых для оценки свертывающих систем.
Фармакодинамические эффекты
У человека наблюдается дозозависимое ингибирование активности фактора Ха. Ривароксабан оказывает дозозависимое влияние на протромбиновое время и близко коррелирует с концентрациями в плазме (r=0,98), если для анализа используется набор Neoplastin. При использовании других реактивов результаты будут отличаться. Протромбиновое время следует измерять в секундах, поскольку МНО (международное нормализованное отношение) откалибровано и сертифицировано только для производных кумарина и не может применяться для других антикоагулянтов.
У пациентов, которым проводятся большие ортопедические операции, 5/95-процентили для протромбинового времени (Neoplastin) через 2-4 часа после приема таблетки (т.е. на максимуме эффекта) варьируют от 13 до 25 секунд.
У пациентов, получающих ривароксабан для лечения и профилактики рецидивов тромбоза глубоких вен (ТГВ) и тромбоэмболии легочной артерии (ТЭЛА), 5/95-процентили для протромбинового времени (Neoplastin) через 2-4 часа после приема таблетки (т.е. на максимуме эффекта) варьируют от 17 до 32 секунд у пациентов, принимающих 15 мг два раза в день, и от 15 до 30 секунд у пациентов, принимающих 20 мг один раз в день.
Также ривароксабан дозозависимо увеличивает активированное частичное тромбопластиновое время (аЧТВ) и результат HepTest; однако эти параметры не рекомендуется использовать для оценки фармакодинамических эффектов ривароксабана.
В период лечения ривароксабаном проводить мониторинг параметров свертывания крови не требуется. Однако если для этого есть клиническое обоснование (например, при передозировке препарата или в случае необходимости экстренного хирургического вмешательства), концентрация ривароксабана может быть измерена при помощи калиброванного количественного теста анти-фактора Xa (например, STA — Liquid Anti-Xa, производитель Диагностика Стаго САС, Франция или аналогичный).
У здоровых мужчин и женщин старше 50 лет удлинение интервала QT под влиянием ривароксабана не наблюдалось.
Фармакокинетика
Всасывание и биодоступность
Ривароксабан быстро всасывается; максимальная концентрация (Стах) достигается через 2-4 часа после приема таблетки.
Абсолютная биодоступность ривароксабана после приема дозы 10 мг высокая (80-100 %) независимо от приема пищи. При приеме ривароксабана в дозе 10 мг с пищей не отмечено изменения AUC (площадь под кривой «концентрация — время») и Сmax (максимальная концентрация). Ривароксабан в дозе 10 мг может назначаться для приема во время еды или независимо от приема пищи.
Фармакокинетика ривароксабана характеризуется умеренной индивидуальной изменчивостью; индивидуальная изменчивость (вариационный коэффициент) составляет от 30 до 40%.
Всасывание ривароксабана зависит от места высвобождения в желудочно-кишечном тракте (ЖКТ). Снижение в 29 % и 56 % в AUC и Cmax, соответственно, в сравнении с приемом целой таблетки, наблюдалось при введении гранулята ривароксабана в проксимальный отдел тонкой кишки. Экспозиция препарата также уменьшается при его введении в дистальный отдел тонкой кишки или восходящую ободочную кишку. Следует избегать введения ривароксабана в желудочно-кишечный тракт дистальнее желудка, поскольку это может повлечь снижение всасывания и, соответственно, экспозиции препарата.
Биодоступность (AUC и Cmax) ривароксабана 20 мг при приеме целой таблетки сопоставима с биодоступностью препарата, принятого внутрь в виде измельченной таблетки (в смеси с яблочным пюре или суспендированной в воде), а также с биодоступностью препарата при введении через желудочный зонд с последующим приемом жидкого питания. Учитывая предсказуемый дозозависимый фармакокинетический профиль ривароксабана, результаты данного исследования биодоступности применимы также и к более низким дозам.
Распределение
В организме человека большая часть ривароксабана (92-95 %) связывается с белками плазмы, основным связывающим компонентом является сывороточный альбумин. Объем распределения — умеренный, Vss составляет приблизительно 50 л.
Метаболизм и выведение
При приеме внутрь приблизительно 2/3 от назначенной дозы ривароксабана подвергается метаболизму и в дальнейшем выводится равными частями почками и через кишечник. Оставшаяся 1/3 дозы выводится посредством прямой почечной экскреции в неизмененном виде, главным образом, за счет активной почечной секреции.
Ривароксабан метаболизируется посредством изоферментов CYP3A4, CYP2J2, а также при помощи механизмов, независимых от системы цитохромов. Основными участками биотрансформации являются окисление морфолиновой группы и гидролиз амидных связей. Согласно данным, полученным in vitro, ривароксабан является субстратом для белков-переносчиков Р-gp (Р-гликопротеина) и Bcrp (белка устойчивости рака молочной железы). Неизмененный ривароксабан является единственным активным соединением в человеческой плазме, значимые или активные циркулирующие метаболиты в плазме не обнаружены. Ривароксабан, системный клиренс которого составляет приблизительно 10 л/ч, может быть отнесен к лекарственным веществам с низким уровнем клиренса. При выведении ривароксабана из плазмы конечный период полувыведения составляет от 5 до 9 часов у молодых пациентов и от 11 до 13 часов — у пожилых пациентов.
Пол/Пожилой возраст (старше 65 лет)
У пожилых пациентов концентрация ривароксабана в плазме выше, чем у молодых пациентов, среднее значение AUC приблизительно в 1,5 раза превышает соответствующие значения у молодых пациентов, главным образом, вследствие кажущегося снижения общего и почечного клиренса (см. раздел «Способ применения и дозы»). Пациентам пожилого возраста коррекция дозы не требуется.
У мужчин и женщин клинически значимых различий фармакокинетики не обнаружено (см. раздел «Способ применения и дозы»).
Масса тела
Слишком малая или большая масса тела (менее 50 кг и более 120 кг) лишь незначительно влияет на концентрацию ривароксабана в плазме (различие составляет менее 25 %) (см. раздел «Способ применения и дозы»). Коррекция дозы препарата в зависимости от массы тела пациента не требуется.
Детский и подростковый возраст (с рождения до 18 лет)
Данные по этой возрастной категории отсутствуют (см. раздел «Способ применения и дозы»).
Межэтнические различия
Клинически значимых различий фармакокинетики и фармакодинамики у пациентов европеоидной, афроамериканской, латиноамериканской, японской или китайской этнической принадлежности не наблюдалось (см. раздел «Способ применения и дозы»).
Пациенты с нарушением функции печени
У пациентов с циррозом печени с легкой степенью печеночной недостаточности (класс А по Чайлд-Пью) фармакокинетика ривароксабана лишь незначительно отличалась (в среднем отмечалось увеличение AUC ривароксабана в 1,2 раза) от соответствующих показателей в контрольной группе здоровых испытуемых. У пациентов с циррозом печени и печеночной недостаточностью средней степени тяжести (класс В по Чайлд-Пью) средняя AUC ривароксабана была значимо повышенной (в 2,3 раза) по сравнению со здоровыми добровольцами. Значение несвязанной AUC было повышено в 2,6 раза. Скорость выведения ривароксабана почками у таких пациентов была снижена также, как и у пациентов со средней степенью почечной недостаточности.
Данные по пациентам с печеночной недостаточностью класса С по классификации Чайлд-Пью отсутствуют.
Подавление активности фактора Ха у пациентов с печеночной недостаточностью средней степени тяжести (класс В по Чайлд-Пью) было выражено сильнее (в 2,6 раза), чем у здоровых добровольцев; протромбиновое время также в 2,1 раза превышало показатели у здоровых добровольцев. Пациенты со среднетяжелой печеночной недостаточностью более чувствительны к ривароксабану, что является следствием более тесной взаимосвязи фармакодинамических эффектов и фармакокинетических параметров, особенно между концентрацией и протромбиновым временем.
Применение препарата Ксарелто® противопоказано у пациентов с заболеваниями печени, протекающими с коагулопатией и клинически значимым риском кровотечения, включая пациентов с циррозом печени классов В и С по классификации Чайлд-Пью (см. разделы «Способ применения и дозы», «Противопоказания»).
Пациенты с нарушением функции почек
У пациентов с нарушением функции почек наблюдалось увеличение площади под кривой концентрация-время ривароксабана, обратно пропорциональное степени снижения почечной функции, оцениваемой по клиренсу креатинина.
У пациентов с легкой (клиренс креатинина 50-80 мл/мин), средней (КлКр 30-49 мл/мин) или тяжелой (КлКр 15-29 мл/мин) степенью почечной недостаточности наблюдалось соответственно 1,4-, 1,5- и 1,6-кратное увеличение концентраций ривароксабана в плазме (AUC) по сравнению со здоровыми добровольцами (см. разделы «Способ применения и дозы», «С осторожностью», «Особые указания»).
Соответствующее увеличение фармакодинамических эффектов было более выраженным.
У пациентов с легкой, средней и тяжелой степенью нарушения функции почек общее подавление активности фактора Ха увеличивалось в 1,5, 1,9 и 2 раза по сравнению со здоровыми добровольцами; протромбиновое время также увеличивалось в 1,3, 2,2 и 2,4 раза, соответственно.
Данные о применении ривароксабана у пациентов с КлКр < 15 мл/мин отсутствуют.
В связи со значительным связыванием с белками плазмы считается, что ривароксабан не будет выводиться с помощью гемодиализа.
Не рекомендуется применять препарат Ксарелто® у пациентов с КлКр < 15 мл/мин (см. раздел «Противопоказания»).
Препарат Ксарелто® следует применять с осторожностью у пациентов с КлКр 15-29 мл/мин. (см. разделы «Способ применения и дозы», «С осторожностью», «Особые указания»).
Показания к применению
Противопоказания
С осторожностью
С осторожностью следует использовать препарат:
Применение при беременности и в период грудного вскармливания
Беременность
Эффективность и безопасность применения ривароксабана у беременных не установлены. Данные, полученные на экспериментальных животных, показали выраженную токсичность ривароксабана для материнского организма, связанную с фармакологическим действием препарата (например, осложнения в форме кровоизлияний) и приводящую к репродуктивной токсичности. Первичного тератогенного потенциала не обнаружено.
Вследствие возможного риска развития кровотечения и способности проникать через плаценту ривароксабан противопоказан при беременности (см. раздел «Противопоказания»).
Женщинам с сохраненной репродуктивной способностью следует использовать эффективные методы контрацепции в период лечения ривароксабаном.
Грудное вскармливание
Эффективность и безопасность применения препарата Ксарелто® у женщин в период грудного вскармливания не установлены.
Данные, полученные на экспериментальных животных, показывают, что ривароксабан выделяется с грудным молоком. Ривароксабан может применяться только после отмены грудного вскармливания (см. раздел «Противопоказания»).
Фертильность
Исследования показали, что ривароксабан не влияет на мужскую и женскую фертильность у крыс. Исследований влияния ривароксабана на фертильность у человека не проводилось.
Способ применения и дозы
Внутрь, независимо от приема пищи.
Если пациент не способен проглотить таблетку целиком, таблетка препарата Ксарелто® может быть измельчена и смешана с водой или жидким питанием, например, яблочным пюре, непосредственно перед приемом внутрь.
Измельченная таблетка препарата Ксарелто® может быть введена через желудочный зонд. Положение зонда в ЖКТ необходимо дополнительно согласовать с врачом перед приемом препарата Ксарелто®. Измельченную таблетку следует вводить через желудочный зонд в небольшом количестве воды, после чего необходимо ввести небольшое количество воды для того, чтобы смыть остатки препарата со стенок зонда.
Профилактика венозной тромбоэмболии (ВТЭ) у пациентов, подвергающихся большим ортопедическим оперативным вмешательствам на нижних конечностях
В целях профилактики ВТЭ при больших ортопедических операциях рекомендуется назначать по 1 таблетке 10 мг 1 раз в день.
Продолжительность лечения:
— 5 недель после большой операции на тазобедренном суставе;
— 2 недели после большой операции на коленном суставе.
Начальную дозу следует принять через 6-10 часов после операции при условии достигнутого гемостаза.
Действия при пропуске приема препарата
В случае пропуска приема препарата пациенту следует принять таблетку препарата Кса-релто® в дозировке 10 мг немедленно и на следующий день продолжить лечение по 1 таблетке в день, как и ранее.
Профилактика рецидивов тромбоза глубоких вен (ТГВ) или тромбоэмболии легочной артерии (ТЭЛА) после как минимум 6 месяцев лечения ТГВ или ТЭЛА
После как минимум 6 месяцев лечения тромбоза глубоких вен или тромбоэмболии легочной артерии рекомендованная доза препарата Ксарелто® составляет 10 мг один раз в день или 20 мг** один раз в день, в зависимости от индивидуального соотношения риска рецидива ТГВ или ТЭЛА и риска кровотечения.
Таблица 1.
| Период | Схема приема | Суммарная суточная доза | |
| Лечение и профилактика рецидивов ТГВ или ТЭЛА | От 1 до 21 дня После 22 дня |
15 мг* два раза в день 20 мг** один раз в день |
30 мг 20 мг |
| Профилактика рецидивов ТГВ и ТЭЛА | После как минимум 6 месяцев лечения ТГВ или ТЭЛА | 10 мг один раз в день или 20 мг** один раз в день |
10 мг или 20 мг |
* в случае необходимости приема препарата в дозе 15 мг следует применять препарат Ксарелто®, выпускаемый в соответствующей дозировке, так как таблетки препарата с дозировкой 10 мг выпускаются без риски.
** в случае необходимости приема препарата в дозе 20 мг следует применять препарат Ксарелто®, выпускаемый в соответствующей дозировке.
Препарат Ксарелто® в дозировках 15 мг и 20 мг следует принимать во время еды, в дозировке 10 мг независимо от приема пищи.
Действия при пропуске приема препарата
Необходимо следовать назначенной схеме приема препарата.
В случае пропуска приема препарата при назначении препарата Ксарелто® в дозировке 15 мг два раза в день следует немедленно принять пропущенную таблетку, чтобы обеспечить прием суммарной суточной дозы препарата, составляющей 30 мг. В этом случае допускается принять две таблетки препарата Ксарелто® в дозировке 15 мг в один прием. На следующий день необходимо продолжить лечение в соответствии с рекомендованной схемой приема препарата.
В случае пропуска приема препарата при назначении препарата Ксарелто® один раз в день следует немедленно принять пропущенную таблетку, чтобы обеспечить прием суточной дозы препарата. На следующий день необходимо продолжить лечение в соответствии с рекомендованной схемой приема препарата.
Отдельные группы пациентов
Коррекция дозы в зависимости от возраста пациента (старше 65 лет), пола, массы тела или этнической группы не требуется.
Безопасность и эффективность применения у детей и подростков до 18 лет не установлены.
Пациенты с нарушением функции печени
Ривароксабан противопоказан пациентам с заболеваниями печени, сопровождающимися коагулопатией, которая обуславливает клинически значимый риск кровотечения (см. раздел «Противопоказания»).
Пациентам с другими заболеваниями печени изменения дозы не требуются (см. раздел «Фармакологические свойства»).
Имеющиеся ограниченные клинические данные, полученные у пациентов со среднетяжелой печеночной недостаточностью (класс B по Чайлд-Пью), указывают на значимое усиление фармакологической активности препарата. У пациентов с тяжелой печеночной недостаточностью (класс С по Чайлд-Пью) клинические данные отсутствуют (см. разделы «Противопоказания», «Фармакологические свойства»).
Пациенты с нарушением функции почек
Имеющиеся ограниченные клинические данные демонстрируют значительное повышение концентраций ривароксабана у пациентов с тяжелой степенью нарушения функции почек (КлКр 15-29 мл/мин). Для лечения этой категории пациентов препарат Ксарелто® следует применять с осторожностью.
Применение ривароксабана не рекомендуется у пациентов с КлКр менее 15мл/мин (см. разделы «Фармакологические свойства», «Противопоказания», «Особые указания»).
Пациентам со средней (КлКр 30-49 мл/мин) или тяжелой (КлКр 15-29 мл/мин) степенью нарушения функции почек следует принимать препарат Ксарелто® в дозе 15 мг два раза в день на протяжении первых трех недель. Впоследствии, когда рекомендуемая доза препарата Ксарелто® составит 20 мг один раз в день, следует предусмотреть снижение дозы до 15 мг один раз в день, если риск возникновения кровотечения выше риска рецидивов ТГВ и ТЭЛА. Рекомендации по применению препарата Ксарелто® в дозе 15 мг основаны на фармакокинетическом моделировании и в клинических исследованиях не изучались (см. разделы «Особые указания», «Фармакологические свойства»).
При применении препарата Ксарелто® в дозировке 10 мг коррекция дозы не требуется. Примечание: Информация о применении препарата Ксарелто® в дозе 10 мг 1 раз в день пациентам с фибрилляцией предсердий неклапанного происхождения, перенесших чрескожное коронарное вмешательство (ЧКВ) с установкой стента и имеющих среднюю степень нарушения функции почек (КлКр 30-49 мл/мин), размещена в инструкции по медицинскому применению лекарственного препарата Ксарелто® 15 / 20 мг (рег. номер ЛП-001457).
Перевод пациентов с лечения антагонистами витамина К (АВК) на препарат Ксарелто®
При переводе пациента с АВК на препарат Ксарелто® значение показателя МНО будет ложно повышаться после приема препарата Ксарелто®. В связи с этим показатель МНО нельзя использовать для контроля антикоагулянтного эффекта препарата Ксарелто® (см. «Взаимодействие с другими лекарственными средствами»).
При профилактике инсульта и системной тромбоэмболии следует прекратить лечение АВК и начать лечение препаратом Ксарелто® при величине МНО ≤ 3,0.
При ТГВ и ТЭЛА следует прекратить лечение АВК и начать лечение препаратом Ксарелто® при величине МНО ≤ 2,5.
Перевод пациентов с препарата Ксарелто® на лечение антагонистами витамина К (АВК)
Существует вероятность недостаточного антикоагулянтного эффекта при переводе пациентов с препарата Ксарелто® на АВК. В переходный период, связанный с переводом на другой противосвертывающий препарат, необходимо обеспечить непрерывный и достаточный антикоагулянтный эффект. Следует иметь в виду, что препарат Ксарелто® может способствовать повышению показателя МНО.
При переводе пациента с препарата Ксарелто® на АВК, оба препарата следует назначать одновременно до тех пор, пока МНО не достигнет значения ≥2,0. В первые два дня переходного периода следует использовать стандартную дозу АВК, а впоследствии руководствоваться значением МНО. В период совместного приема Ксарелто® и АВК МНО следует определять не ранее, чем через 24 часа (после предыдущей, но до приема следующей дозы Ксарелто®). После отмены препарата Ксарелто® определение МНО с достаточной степенью надежности возможно через 24 часа после приема последней дозы препарата (см. «Взаимодействие с другими лекарственными средствами «).
Перевод пациентов с парентеральных антикоагулянтов на препарат Ксарелто®
При переводе пациента с парентеральных антикоагулянтов на препарат Ксарелто® прием препарата Ксарелто® следует начать за 0-2 часа до предполагаемого введения следующей дозы парентерального препарата (например, низкомолекулярного гепарина) или во время отмены длительно применяемого парентерального препарата (например, внутривенного не-фракционированного гепарина).
Перевод пациентов с препарата Ксарелто® на парентеральные антикоагулянты
Прекратить прием препарата Ксарелто® и ввести первую дозу парентерального антикоагулянта во время предполагаемого приема следующей дозы препарата Ксарелто®.
Побочное действие
Безопасность препарата Ксарелто® оценивалась в тринадцати исследованиях III фазы, включавших 53103 пациента, принимавших препарат Ксарелто®.
Таблица 2.
Число пациентов, участвовавших в исследовании и принявших как минимум 1 дозу ривароксабана, суммарная суточная доза и максимальная продолжительность лечения в клинических исследованиях III фазы с использованием препарата Ксарелто® указаны в таблице ниже:
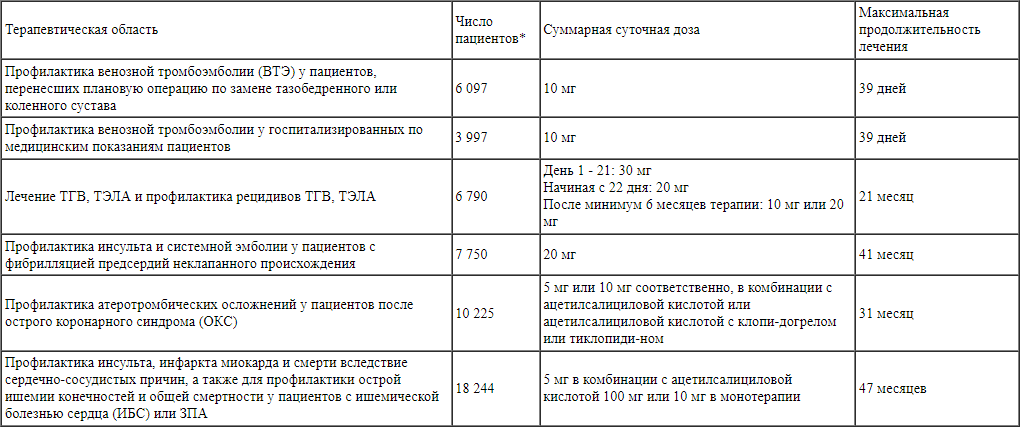
* Пациенты, получившие по меньшей мере одну дозу ривароксабана.
Таблица 3.
Частота возникновения кровотечений и анемии у пациентов, получавших лечение препаратом Ксарелто® в клинических исследованиях III фазы.
|
Показание к применению |
Количество пациентов |
|
| Любое кровотечение | Анемия | |
| Профилактика венозной тромбоэмболии (ВТЭ) у пациентов, перенесших плановую операцию по замене тазобедренного или коленного сустава | 6,8 % | 5,9 % |
| Профилактика венозной тромбоэмболии у госпитализированных по медицинским показаниям пациентов | 12,6 % | 2,1 % |
| Лечение ТГВ, ТЭЛА и профилактика рецидивов ТГВ, ТЭЛА | 23 % | 1,6 % |
| Профилактика инсульта и системной тромбоэмболии у пациентов с фибрилляцией предсердий неклапанного происхождения | 28 событий на 100 пациенто-лет | 2,5 события на 100 пациенто-лет |
| Профилактика атеротромбических осложнений у пациентов после острого коронарного синдрома (ОКС) | 22 события на 100 пациенто-лет | 1,4 события на 100 пациенто-лет |
| Профилактика инсульта, инфаркта миокарда и смерти вследствие сердечно-сосудистых причин, а также для профилактики острой ишемии конечностей и общей смертности у пациентов с ИБС или ЗПА | 6,7 события на 100 пациенто-лет | 0,15 события на 100 пациенто-лет* |
* При сборе данных о нежелательных явлениях применялся предустановленный выборочный подход
Учитывая механизм действия, применение препарата Ксарелто® может сопровождаться повышенным риском скрытого или явного кровотечения из любых органов и тканей, которое может приводить к постгеморрагической анемии. Риск развития кровотечений может увеличиваться у пациентов с неконтролируемой артериальной гипертензией и/или при совместном применении с препаратами, влияющими на гемостаз (см. раздел «С осторожностью»). Признаки, симптомы и степень тяжести (включая возможный летальный исход) варьируют в зависимости от локализации, степени тяжести или продолжительности кровотечения и/или анемии (см. раздел «Передозировка»).
Геморрагические осложнения могут проявляться в виде слабости, бледности, головокружения, головной боли или необъяснимых отеков, одышки или шока, развитие которого нельзя объяснить другими причинами. В некоторых случаях вследствие анемии развивались симптомы ишемии миокарда, такие как боль в груди и стенокардия.
При применении препарата Ксарелто® регистрировались и такие известные осложнения, вторичные по отношению к тяжелым кровотечениям, как синдром повышенного субфасциального давления (компартмент-синдром) и почечная недостаточность вследствие гипоперфузии. Таким образом, следует учитывать возможность кровотечения при оценке состояния любого пациента, получающего антикоагулянты.
Частота встречаемости НЛР (нежелательных лекарственных реакций) при использовании препарата Ксарелто® приведена в таблице ниже. В рамках каждой группы, выделенной по частоте, нежелательные явления представлены в порядке уменьшения их серьезности.
Частота встречаемости определяется как:
очень часто (≥ 1/10),
часто (от ≥ 1/100 до < 1/10),
нечасто (от ≥ 1/1000 до < 1/100),
редко (от ≥ 1/10000 до < 1/1000).
Таблица 4:
Все возникшие на фоне лечения нежелательные лекарственные реакции, зарегистрированные у пациентов в клинических исследованиях III фазы (кумулятивные данные RECORD 1-4, ROCKET AF, J-ROCKET, MAGELLAN, ATLAS, EINSTEIN (DVT/PE/Extension/CHOICE) и COMPASS*)
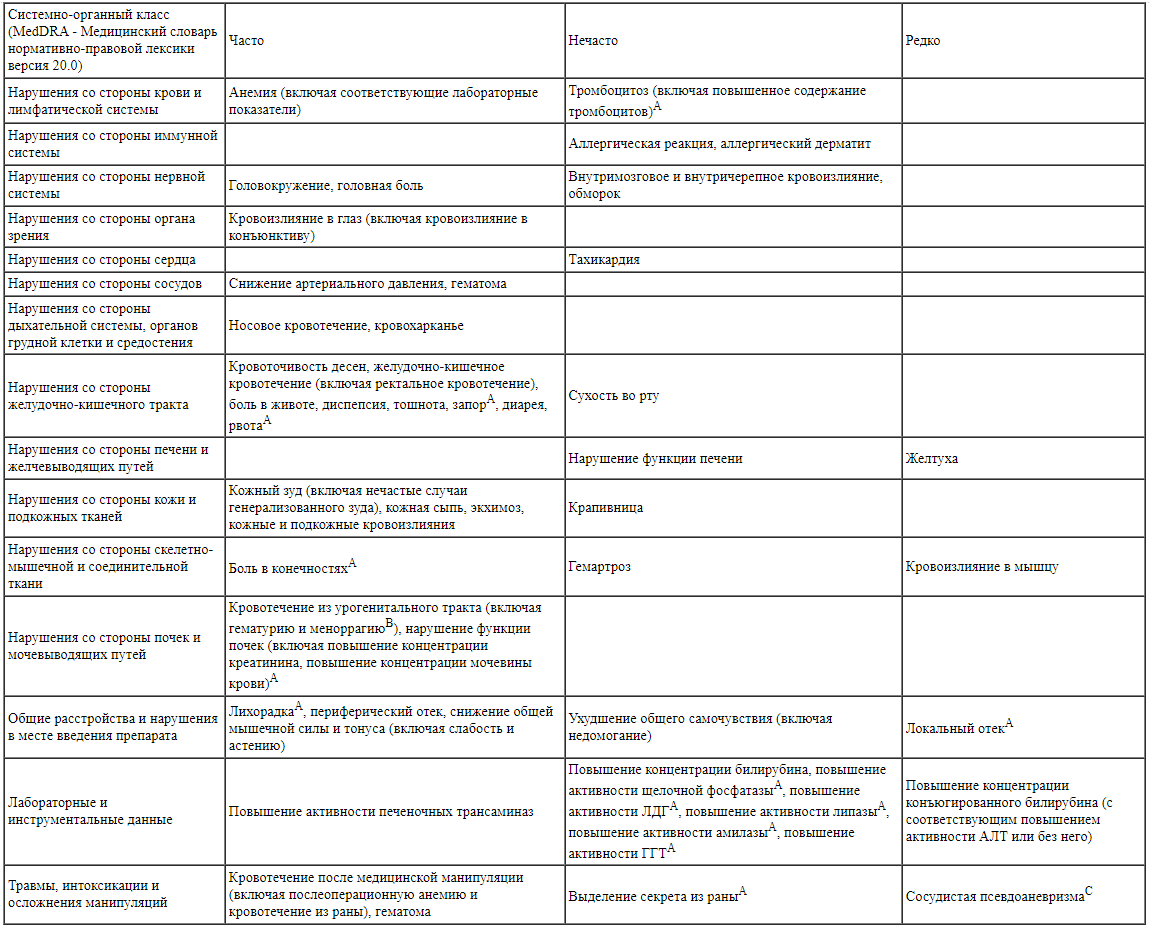
А наблюдались после больших ортопедических операций на нижних конечностях
В регистрировались при лечении ВТЭ как очень частые у женщин моложе 55 лет
С регистрировались как нечастые в рамках профилактики осложнений при ОКС (после проведения чрескожных вмешательств).
* Применялся предварительно заданный избирательный подход к сбору данных по нежелательным явлениям. Так как частота нежелательных лекарственных реакций не повысилась, и так как никаких новых нежелательных лекарственных реакций идентифицировано не было, данные из исследования COMPASS не были включены для расчета частоты в данной таблице.
Во время пострегистрационного мониторинга сообщалось о случаях приведенных ниже нежелательных реакций, развитие которых имело временную связь с приемом препарата Ксарелто®. Оценить частоту встречаемости таких нежелательных реакций в рамках пострегистрационного мониторинга не представляется возможным.
Нарушения со стороны иммунной системы: ангионевротический отек, аллергический отек. В рамках регистрационных клинических исследований (РКИ) III фазы такие нежелательные реакции были расценены как нечастые (от ≥1/1000 до <1/100).
Нарушения со стороны печени и желчевыводящих путей: холестаз, гепатит (включая гепатоцеллюлярное повреждение). В рамках РКИ III фазы такие нежелательные реакции были расценены как редкие (от ≥1/10000 до <1/1000).
Нарушения со стороны кровеносной и лимфатической системы: тромбоцитопения. В рамках РКИ III фазы такие нежелательные реакции были расценены как нечастые (от ≥1/1000 до <1/100).
Передозировка
Сообщалось о редких случаях передозировки до 600 мг без осложнений в виде кровотечения или других нежелательных реакций. Вследствие ограниченного всасывания ожидается эффект насыщения без дальнейшего повышения среднего содержания ривароксабана в плазме при гипертерапевтических дозах в 50 мг или выше.
Специфический антидот ривароксабана неизвестен. В случае передозировки для снижения всасывания ривароксабана можно использовать активированный уголь. Учитывая интенсивное связывание с белками плазмы, ожидается, что ривароксабан не будет выводиться при проведении диализа.
Лечение кровотечений
При возникновении осложнения в виде кровотечения следующий прием препарата должен быть отложен или лечение должно быть отменено, в зависимости от ситуации. Период полувыведения ривароксабана составляет приблизительно 5-13 часов. Лечение следует подбирать индивидуально, в соответствии с тяжестью и локализацией кровотечения.
При необходимости может применяться соответствующее симптоматическое лечение, например, механическая компрессия (например, в случае сильного носового кровотечения), хирургический гемостаз с процедурами контроля за кровотечением, восполнение объема жидкости и гемодинамическая поддержка, применение препаратов крови (эритроцитарной массы или свежезамороженной плазмы, в зависимости от сопутствующей анемии или коагулопатии) или тромбоцитов.
Если перечисленные выше мероприятия не приводят к устранению кровотечения, может быть назначен специфический прокоагулянт, например концентрат протромбинового комплекса, концентрат активированного протромбинового комплекса или рекомбинантный фактор VIIa (rf VIIa). Однако до настоящего времени опыт применения этих препаратов при лечении пациентов, получающих ривароксабан, очень ограничен.
Ожидается, что протамина сульфат и витамин К не будут оказывать влияния на противосвертывающую активность ривароксабана.
Имеется ограниченный опыт применения транексамовой кислоты и отсутствует опыт применения аминокапроновой кислоты и апротинина у пациентов, получающих препарат Ксарелто®. Научное обоснование целесообразности или опыт использования системного гемостатического препарата десмопрессин у пациентов, получающих препарат Ксарелто®, отсутствует.
Взаимодействие с другими лекарственными средствами
Фармакокинетические взаимодействия
Выведение ривароксабана осуществляется главным образом посредством метаболизма в печени, опосредованного системой цитохрома Р450 (CYP3A4, CYP2J2), а также — путем почечной экскреции неизмененного лекарственного вещества с использованием систем переносчиков P-gp/Bcrp (Р-гликопротеина/белка устойчивости рака молочной железы) (см. раздел «Фармакокинетика»).
Ингибирование CYP
Ривароксабан не ингибирует CYP 3A4 или любые другие основные изоформы CYP.
Индукция CYP
Ривароксабан не индуцирует CYP 3A4 или любые другие основные изоформы CYP.
Влияние на ривароксабан
Одновременное применение ривароксабана и мощных ингибиторов изофермента CYP3A4 и Р-гликопротеина может привести к снижению почечного и печеночного клиренса и, таким образом, значимо увеличить системное воздействие.
Совместное применение ривароксабана и азолового противогрибкового средства кетоконазола (400 мг 1 раз в день), являющегося мощным ингибитором CYP3A4 и Р-гликопротеина, приводило к повышению средней равновесной AUC ривароксабана в 2,6 раза и увеличению средней Стах ривароксабана в 1,7 раза, что сопровождалось значимым усилением фармакодинамических эффектов препарата.
Совместное назначение ривароксабана и ингибитора протеазы ВИЧ ритонавира (600 мг 2 раза в день), являющегося мощным ингибитором CYP3A4 и Р-гликопротеина, приводило к увеличению средней равновесной AUC ривароксабана в 2,5 раза и увеличению средней Стах ривароксабана в 1,6 раза, что сопровождалось значимым усилением фармакодинамических эффектов препарата.
В связи с этим ривароксабан не рекомендуется к применению у пациентов, получающих системное лечение противогрибковыми препаратами азоловой группы или ингибиторами протеазы ВИЧ (см. разделы «С осторожностью», «Особые указания»).
Ожидается, что другие лекарственные вещества, сильно угнетающие только один из путей выведения ривароксабана — с участием CYP3A4 или Р-гликопротеина, будут увеличивать концентрацию ривароксабана в плазме до менее значимых значений.
Кларитромицин (500 мг 2 раза в день), мощный ингибитор изофермента CYP3A4 и умеренный ингибитор Р-гликопротеина, вызывал увеличение значений AUC в 1,5 раза и Стах ривароксабана в 1,4 раза. Это увеличение имеет порядок нормальной изменчивости AUC и Стах и считается клинически незначимым.
Эритромицин (500 мг 3 раза в день), умеренно подавляющий изофермент CYP3A4 и Р-гликопротеин, вызывал увеличение значений AUC и Стах ривароксабана в 1,3 раза. Это увеличение имеет порядок нормальной изменчивости AUC и Сmах и считается клинически незначимым.
У пациентов с легкой степенью нарушения функции почек (КлКр 50-80 мл/мин) эритромицин (500 мг 3 раза в день) вызывал увеличение значений AUC ривароксабана в 1,8 раза и Стах в 1,6 раза по сравнению с пациентами с нормальной функцией почек, не получавших сопутствующей терапии. У пациентов со средней степенью нарушения функции почек (КлКр 30-49 мл/мин) эритромицин вызывал увеличение значений AUC ривароксабана в 2,0 раза и Стах в 1,6 раза по сравнению с пациентами с нормальной функцией почек, не получавших сопутствующей терапии (см. раздел «С осторожностью»).
Флуконазол (400 мг 1 раз в день), умеренно подавляющий изофермент CYP3A4, вызывал увеличение значений AUC в 1,4 раза и Стах ривароксабана в 1,3 раза. Это увеличение имеет порядок нормальной изменчивости AUC и Стах и считается клинически незначимым.
Следует избегать одновременного применения ривароксабана с дронедароном в связи с ограниченностью клинических данных о совместном применении.
Совместное назначение ривароксабана и рифампицина, являющегося мощным индуктором CYP3A4 и Р-гликопротеина, приводило к снижению средней AUC ривароксабана приблизительно на 50 % и параллельному уменьшению его фармакодинамических эффектов. Совместное применение ривароксабана с другими мощными индукторами CYP3A4 (например, фенитоином, карбамазепином, фенобарбиталом или препаратами Зверобоя продырявленного) также может привести к снижению концентраций ривароксабана в плазме. Уменьшение концентраций ривароксабана в плазме признано клинически незначимым. Мощные индукторы CYP3A4 необходимо применять с осторожностью.
Фармакодинамические взаимодействия
После одновременного применения эноксапарина натрия (однократная доза 40 мг) и ривароксабана (однократная доза 10 мг) наблюдался суммационный эффект в отношении активности анти-фактора Ха, не сопровождавшийся дополнительными суммационными эффектами в отношении проб на свертываемость крови (протромбиновое время, аЧТВ). Эноксапарин натрия не изменял фармакокинетику ривароксабана.
После совместного назначения ривароксабана в дозе 15 мг и напроксена в дозе 500 мг клинически значимого удлинения времени кровотечения не наблюдалось. Тем не менее, у отдельных лиц возможен более выраженный фармакодинамический ответ.
Не обнаружено фармакокинетического взаимодействия между ривароксабаном в дозе 15 мг и клопидогрелом (ударная доза 300 мг с последующим назначением поддерживающих доз 75 мг), но у части пациентов обнаружено значимое увеличение времени кровотечения, не коррелировавшее с агрегацией тромбоцитов и содержанием Р-селектина или GPIIb/IIIa-рецептора.
Перевод пациентов с варфарина (МНО от 2,0 до 3,0) на ривароксабан (20 мг) или с ривароксабана (20 мг) на варфарин (МНО от 2,0 до 3,0) сопровождался более чем аддитивным увеличением протромбинового времени / МНО (Неопластин) (в отдельных случаях до 12), тогда как эффекты изменения аЧТВ, подавления активности фактора Xa и эндогенного потенциала тромбина (ЭПТ) были аддитивными.
Для оценки фармакодинамических эффектов препарата Ксарелто® в переходный период можно провести анализ анти-Ха факторной активности, PiCT и HepTest, если на определяемые в их ходе показатели не повлиял варфарин.
Начиная с 4-го дня после отмены варфарина, все анализы (включая ПВ, аЧТВ, подавление активности фактора Xa и ЭПТ) отражали исключительно эффект препарата Ксарелто® (см. раздел «Способ применения и дозы»).
Для оценки фармакодинамических эффектов варфарина в переходный период можно использовать показатель МНО, измеренный в момент достижения Cmin ривароксабана (через 24 часа после приема дозы ривароксабана), так как в этот момент времени влияние ривароксабана на результаты анализа минимально.
Фармакокинетического взаимодействия между варфарином и препаратом Ксарелто® не обнаружено.
Лекарственное взаимодействие препарата Ксарелто® с антагонистом витамина К (АВК) фениндионом не изучалось. Рекомендуется по мере возможности избегать перевода пациентов с терапии препаратом Ксарелто® на терапию АВК фениндионом и наоборот.
Имеется ограниченный опыт перевода пациентов с терапии АВК аценокумаролом на препарат Ксарелто®.
Если возникает необходимость перевести пациента с терапии препаратом Ксарелто® на терапию АВК фениндионом или аценокумаролом, то следует соблюдать особую осторожность, в период совместного приема препарата Ксарелто® и АВК ежедневный контроль фармакодинамического действия препаратов (МНО, протромбиновое время) должен проводиться непосредственно перед приемом следующей дозы Ксарелто®.
Если возникает необходимость перевести пациента с терапии АВК фениндионом или аценокумаролом на терапию препаратом Ксарелто®, то следует соблюдать особую осторожность, контроль фармакодинамического действия препаратов при этом не требуется.
Как и в случае применения других антикоагулянтов, необходимо соблюдать осторожность при совместном применении препарата Ксарелто® с селективными ингибиторами обратного захвата серотонина (СИОЗС) и селективными ингибиторами обратного захвата серотонина и норэпинефрина (СИОЗСН), поскольку применение этих препаратов повышает риск кровотечения. Результаты клинических исследований продемонстрировали численное повышение больших и небольших клинически значимых кровотечений во всех группах лечения при совместном применении этих препаратов.
Сопутствующее применение других препаратов
Не отмечалось клинически значимых фармакокинетических или фармакодинамических взаимодействий при одновременном применении ривароксабана с мидазоламом (субстратом CYP3A4), дигоксином (субстратом Р-гликопротеина) или аторвастатином (субстратом CYP3A4 и P-gp).
Совместное применение с ингибитором протонной помпы омепразолом, антагонистом Н2-рецепторов ранитидином, антацидами алюминия гидроксидом / магния гидроксидом, напроксеном, клопидогрелом или эноксапарином не влияет на биодоступность и фармакокинетику ривароксабана.
Не наблюдалось никаких клинически значимых фармакокинетических или фармакодинамических взаимодействий при совместном применении Ксарелто® и 500 мг ацетилсалициловой кислоты.
Продукты питания и молочные продукты
Препарат Ксарелто® в дозировке 10 мг можно принимать независимо от приема пищи (см. раздел “Фармакологические свойства”).
Влияние на лабораторные параметры
Влияние на результаты проб на параметры свертывания (протромбиновое время, аЧТВ, HepTest) соответствует ожидаемому с учетом механизма действия препарата Ксарелто®.
Особые указания
Применение сопутствующих препаратов
Применение ривароксабана не рекомендуется у пациентов, получающих сопутствующее системное лечение азоловыми противогрибковыми препаратами (например, кетоконазолом) или ингибиторами ВИЧ-протеаз (например, ритонавиром). Эти препараты являются мощными ингибиторами CYP3A4 и Р-гликопротеина. Таким образом, эти препараты могут повышать концентрацию ривароксабана в плазме крови до клинически значимых значений (в 2,6 раза в среднем), что может привести к повышенному риску кровотечений (см. разделы «С Осторожностью», «Взаимодействие с другими лекарственными средствами»).
Однако, азоловый противогрибковый препарат флуконазол, умеренный ингибитор CYP3A4, оказывает менее выраженное влияние на экспозицию ривароксабана и может применяться с ним одновременно (см. раздел «Взаимодействие с другими лекарственными средствами»).
Нарушение функции почек
Ривароксабан следует с осторожностью применять у пациентов со средней степенью нарушения функции почек (КлКр 30-49 мл/мин), получающих сопутствующие препараты, которые могут приводить к повышению концентрации ривароксабана в плазме (см. разделы «С осторожностью», «Взаимодействие с другими лекарственными средствами»).
У пациентов с тяжелой степенью нарушения функции почек (КлКр < 30 мл/мин) концентрация ривароксабана в плазме может быть значимо повышена (в 1,6 раза в среднем), что может привести к повышенному риску кровотечений. Вследствие основного заболевания для этих пациентов повышен риск как кровотечения, так и тромбоза. В связи с ограниченным количеством клинических данных, препарат Ксарелто® должен применяться с осторожностью у пациентов с КлКр 15-29 мл/мин.
Клинические данные о применении ривароксабана у пациентов с тяжелым нарушением функции почек (КлКр <15 мл/мин) отсутствуют. Поэтому применение препарата Ксарелто® у таких пациентов не рекомендуется (см. разделы «Противопоказания», «Способ применения и дозы», «Фармакологические свойства»).
За пациентами с тяжелым нарушением функции почек (КлКр 15-29 мл/мин) или повышенным риском кровотечения, а также пациентами, получающими сопутствующее системное лечение азоловыми противогрибковыми препаратами или ингибиторами ВИЧ-протеаз, необходимо проводить тщательное наблюдение на предмет наличия признаков кровотечения после начала лечения.
Наблюдение может осуществляться путем проведения регулярного физикального обследования пациентов, тщательного контроля за состоянием дренажа послеоперационной раны, а также путем периодического определения гемоглобина.
Оперативные вмешательства при переломе проксимальных отделов бедренной кости
Применение препарата Ксарелто® при оперативных вмешательствах по поводу перелома проксимальных отделов бедренной кости не изучалось в интервенционных клинических исследованиях. Имеются ограниченные клинические данные, полученные в наблюдательных исследованиях, у пациентов, подвергающихся оперативным вмешательствам при переломе нижних конечностей, в том числе, при переломе проксимальных отделов бедренной кости.
Риск кровотечения
Как и при приеме других антикоагулянтов необходимо тщательно наблюдать пациентов, принимающих препарат Ксарелто®, для выявления признаков кровотечения.
В случае тяжелого кровотечения прием препарата Ксарелто® должен быть прекращен.
В клинических исследованиях кровотечения из слизистых оболочек (а именно: кровотечение из носа, десен, желудочно-кишечного тракта, мочеполовой системы, включая аномальное вагинальное или усиленное менструальное кровотечение) и анемия наблюдались чаще при длительном лечении ривароксабаном по сравнению с лечением АВК. Таким образом, в дополнение к надлежащему клиническому наблюдению, лабораторное исследование гемоглобина/гематокрита может быть значимым для выявления скрытых кровотечений и количественной оценки клинической значимости явных кровотечений, которые будут сочтены допустимыми.
Препарат Ксарелто®, как и другие антитромботические средства, следует с осторожностью применять при лечении пациентов, имеющих повышенный риск кровотечений, в том числе:
Следует соблюдать осторожность, если пациент одновременно получает лекарственные препараты, влияющие на гемостаз, такие как нестероидные противовоспалительные препараты (НПВП), ингибиторы агрегации тромбоцитов, другие антитромботические препараты или селективные ингибиторы обратного захвата серотонина (СИОЗС) и селективные ингибиторы обратного захвата серотонина и норэпинефрина (СИОЗСН) (см. раздел «Взаимодействие с другими лекарственными средствами»).
У пациентов с риском развития язвенной болезни желудка и 12-перстной кишки может быть назначено соответствующее профилактическое лечение.
При необъяснимом снижении гемоглобина или артериального давления необходимо искать источник кровотечения.
Терапия ривароксабаном не требует рутинного мониторинга его экспозиции. Тем не менее измерение концентрации ривароксабана с помощью калиброванного теста для количественного определения анти-Ха активности, может оказаться полезным в исключительных случаях, когда информация об экспозиции ривароксабана может быть использована при принятии клинически значимых решений, например, в случае передозировки или экстренного хирургического вмешательства.
Удлинение корригированного интервала QT
На фоне лечения ривароксабаном удлинения интервала QT не наблюдалось.
Спинальная анестезия
При выполнении эпидуральной/спинальной анестезии или спинномозговой пункции у пациентов, получающих ингибиторы агрегации тромбоцитов с целью профилактики тромбоэмболических осложнений, существует риск развития эпидуральной или спинномозговой гематомы, которая может привести к длительному параличу.
Риск этих событий в дальнейшем повышается при использовании постоянных катетеров или сопутствующем применении лекарственных препаратов, влияющих на гемостаз. Травма при выполнении эпидуральной или спинномозговой пункции или повторная пункция также могут способствовать повышению риска.
Пациенты должны находиться под наблюдением для выявления признаков или симптомов неврологических нарушений (например, онемение или слабость ног, дисфункция кишечника или мочевого пузыря). При обнаружении неврологических расстройств необходима срочная диагностика и лечение.
Врач должен сопоставить потенциальную пользу и риск перед проведением спинномозгового вмешательства пациентам, получающим антикоагулянты или готовящимся к получению антикоагулянтов с целью профилактики тромбоза.
С целью снижения потенциального риска кровотечения, ассоциированного с одновременным применением ривароксабана и выполнением эпидуральной/спинальной анестезии или спинальной пункции, следует учитывать фармакокинетический профиль ривароксабана. Установку или удаление эпидурального катетера или люмбальную пункцию лучше проводить тогда, когда антикоагулянтный эффект ривароксабана оценивается как слабый.
Эпидуральный катетер извлекают не ранее чем через 18 часов после назначения последней дозы препарата Ксарелто®.
Препарат Ксарелто® не следует назначать ранее чем через 6 часов после извлечения эпидурального катетера.
В случае травматичной пункции назначение препарата Ксарелто® следует отложить на 24 часа.
Хирургические операции и вмешательства
Если необходимо проведение инвазивной процедуры или хирургического вмешательства, прием препарата Ксарелто® следует прекратить по крайней мере за 24 часа до вмешательства, если это возможно, и на основании заключения врача.
Если процедуру нельзя отложить, повышенный риск кровотечения следует оценивать в сравнении с необходимостью срочного вмешательства.
Прием препарата Ксарелто® следует возобновить после инвазивной процедуры или хирургического вмешательства, при условии наличия соответствующих клинических показателей и адекватного гемостаза (см. раздел «Фармакологические свойства»)
Женщины репродуктивного возраста
Препарат Ксарелто® можно использовать женщинам детородного возраста только при условии применения эффективных методов контрацепции.
Кожные реакции
При проведении постмаркетинговых наблюдений сообщалось о случаях возникновения синдрома Стивенса-Джонсона и токсического эпидермального некролиза. При первом появлении тяжелой кожной сыпи (например, при ее распространении, интенсификации и/или образовании волдырей) или при наличии других симптомов гиперчувствительности, связанных с поражением слизистой оболочки, следует прекратить терапию препаратом Ксарелто®.
Пациенты с искусственными клапанами сердца
Основываясь на данных рандомизированного контролируемого клинического исследования по сравнению терапии препаратом Ксарелто® и антитромбоцитарной терапии, применение препарата Ксарелто® не рекомендуется для профилактики тромбозов у пациентов, перенесших недавнюю транскатетерную замену аортального клапана (TAVR). Безопасность и эффективность применения препарата Ксарелто® не изучались у пациентов с какими-либо другими искусственными клапанами сердца или у пациентов после иных вмешательств на клапанах сердца, следовательно, нет данных, подтверждающих, что применение препарата Ксарелто® обеспечивает достаточный антикоагулянтный эффект у данных категорий пациентов.
Пациенты с высоким риском тройного позитивного антифосфолипидного синдрома
Применение препарата Ксарелто® не рекомендуется у пациентов, имеющих тромбозы в анамнезе, у которых диагностирован устойчивый тройной позитивный антифосфолипидный синдром (наличие волчаночного антикоагулянта, антител к кардиолипину и антител к бета-2-гликопротеину I), поскольку терапия ривароксабаном сопровождается повышенной частотой рецидивов тромботических событий в сравнении с терапией антагонистами витамина К (АВК).
Пациенты с гемодинамически нестабильной тромбоэмболией легочной артерии (ТЭЛА) и пациенты, которым требуется проведение тромболизиса или тромбэктомии
Ривароксабан не рекомендуется в качестве альтернативы нефракционированному гепарину у пациентов с гемодинамически нестабильной тромбоэмболией легочной артерии, а также у пациентов, которые могут нуждаться в проведении тромболизиса или тромбэктомии, поскольку безопасность и эффективность препарата Ксарелто® при таких клинических ситуациях не установлена.
Данные по безопасности, полученные из доклинических исследований
За исключением эффектов, связанных с усилением фармакологического действия (кровотечений), при анализе доклинических данных, полученных в исследованиях по фармакологической безопасности, специфической опасности для человека не обнаружено.
Влияние на способность управлять транспортными средствами, механизмами
При применении препарата Ксарелто® отмечались случаи обмороков и головокружения, которые могут влиять на способность управления транспортными средствами или другими механизмами (см. раздел «Побочное действие»). Пациентам, у которых возникают данные неблагоприятные реакции, не следует управлять транспортными средствами или другими механизмами.
Форма выпуска
Таблетки покрытые пленочной оболочкой 10 мг.
По 5, 10 или 14 таблеток в блистеры из Ал/ПП или Ал/ПВХ-ПВДХ.
1 блистер с 5 таблетками, 1, 3 или 10 блистеров с 10 таблетками, 2 или 7 блистеров с 14 таблетками вместе с инструкцией по применению в картонную пачку с контролем первого вскрытия.
Условия хранения
При температуре не выше 30 °С.
Хранить в недоступном для детей месте.
Срок годности
3 года
Не применять по истечении срока годности.
Условия отпуска
Отпускается по рецепту.
Владелец регистрационного удостоверения
Байер АГ, Кайзер-Вильгельм-Аллее, 1, 51373 Леверкузен, Германия
Bayer AG, Kaiser-Wilhelm-Allee, 1,
51373 Leverkusen, Germany
Производители
Производство готовой лекарственной формы
Байер АГ, Кайзер-Вильгельм-Аллее, 51368 Леверкузен, Германия
Bayer AG, Kaiser-Wilhelm-Allee, 51368 Leverkusen, Germany
Первичная упаковка
Байер АГ, Кайзер-Вильгельм-Аллее, 51368 Леверкузен, Германия
Bayer AG, Kaiser-Wilhelm-Allee, 51368 Leverkusen, Germany
Вторичная/потребительская упаковка
Байер АГ, Кайзер-Вильгельм-Аллее, 51368 Леверкузен, Германия
Bayer AG, Kaiser-Wilhelm-Allee, 51368 Leverkusen, Germany
или
Штегеманн Лонферпакунг унд Логистишер Сервис е.К., Уп’н Ниен-Эш 14, Гревен, 48268, Германия
Stegemann Lohnverpackung & Logistischer Service e.K., Up’n Nien Esch 14, 48268 Greven, Germany
Выпускающий контроль качества
Байер АГ, Кайзер-Вильгельм-Аллее, 51368 Леверкузен, Германия
Bayer AG, Kaiser-Wilhelm-Allee, 51368 Leverkusen, Germany
Организация, принимающая претензии от потребителей:
АО «БАЙЕР»
107113 Москва, 3-я Рыбинская ул., д. 18, стр. 2
Купить Ксарелто 10 мг в ГорЗдрав
Купить Ксарелто 10 мг в megapteka.ru
Купить Ксарелто 10 мг в Планета Здоровья
*Цены в Москве. Точная цена в Вашем городе будет указана на сайте аптеки.
Комментарии
(видны только специалистам, верифицированным редакцией МЕДИ РУ)
Ксарелто® (Xarelto®)
💊 Состав препарата Ксарелто®
✅ Применение препарата Ксарелто®
Препарат отпускается по рецепту
Входит в список «Жизненно необходимых и важнейших лекарственных
препаратов»
Температура хранения: от 2 до 30 °С
Описание активных компонентов препарата
Ксарелто®
(Xarelto®)
Приведенная научная информация является обобщающей и не может быть использована для принятия
решения о возможности применения конкретного лекарственного препарата.
Дата обновления: 2024.12.05
Владелец регистрационного удостоверения:
Код ATX:
B01AF01
(Ривароксабан)
Лекарственная форма
|
Препарат отпускается по рецепту |
Ксарелто® |
Таблетки, покрытые пленочной оболочкой, 10 мг: 5, 10, 28, 30, 98 или 100 шт. рег. №: ЛСР-009820/09 |
Форма выпуска, упаковка и состав
препарата Ксарелто®
Таблетки, покрытые пленочной оболочкой розового цвета, круглые, двояковыпуклые; методом выдавливания нанесена гравировка: на одной стороне — треугольник с обозначением дозировки «10», на другой — фирменный байеровский крест.
Вспомогательные вещества: целлюлоза микрокристаллическая — 40 мг, кроскармеллоза натрия — 3 мг, гипромеллоза 5 cP (гидроксипропилметилцеллюлоза 2910) — 3 мг, лактозы моногидрат — 27.9 мг, магния стеарат — 0.6 мг, натрия лаурилсульфат — 0.5 мг.
Состав оболочки: краситель железа оксид красный — 0.015 мг, гипромеллоза 15 cP (гидроксипропилметилцеллюлоза 2910) — 1.5 мг, макрогол 3350 (полиэтиленгликоль (3350)) — 0.5 мг, титана диоксид — 0.485 мг.
5 шт. — блистеры (1) — пачки картонные с контролем первого вскрытия.
10 шт. — блистеры (1) — пачки картонные с контролем первого вскрытия.
10 шт. — блистеры (3) — пачки картонные с контролем первого вскрытия.
10 шт. — блистеры (10) — пачки картонные с контролем первого вскрытия.
14 шт. — блистеры (2) — пачки картонные с контролем первого вскрытия.
14 шт. — блистеры (7) — пачки картонные с контролем первого вскрытия.
Фармакологическое действие
Высокоселективный прямой ингибитор фактора Ха.
Активация фактора X с образованием фактора Ха через внутренний и внешний пути свертывания играет центральную роль в коагуляционном каскаде. Фактор Ха является компонентом формирующегося протромбиназного комплекса, действие которого приводит к превращению протромбина в тромбин. В результате эти реакции приводят к формированию фибринового тромба и активации тромбоцитов тромбином. Одна молекула фактора Ха катализирует образование более 1000 молекул тромбина, что получило название «тромбинового взрыва». Скорость реакции связанного в протромбиназе фактора Ха увеличивается в 300000 раз по сравнению с таковой свободного фактора Ха, что обеспечивает резкий скачок в уровне тромбина. Селективные ингибиторы фактора Ха могут остановить «тромбиновый взрыв». Таким образом, ривароксабан оказывает влияние на результаты некоторых специфических или общих лабораторных исследований, применяемых для оценки свертывающих систем.
У человека наблюдалось дозозависимое ингибирование фактора Ха. Ривароксабан оказывает дозозависимое влияние на протромбиновое время и близко коррелирует с концентрациями в плазме (r=0.98), если для анализа используется набор Neoplastin. При использовании других реактивов результаты будут отличаться. Протромбиновое время следует измерять в секундах, поскольку MHO откалибровано и сертифицировано только для производных кумарина и не может применяться для других антикоагулянтов.
У пациентов, которым проводятся большие ортопедические операции, 5/95-процентили для протромбинового времени (Neoplastin) через 2-4 ч после приема таблетки (т.е. на максимуме эффекта) варьируют от 13 до 25 сек.
У пациентов, получающих ривароксабан для лечения и профилактики рецидивов тромбоза глубоких вен (ТГВ) и тромбоэмболии легочной артерии (ТЭЛА), 5/95-процентили для протромбинового времени (Neoplastin) через 2-4 ч после приема таблетки (т.е. на максимуме эффекта) варьируют от 17 до 32 сек у пациентов, принимающих 15 мг 2 раза/сут, и от 15 до 30 сек у пациентов, принимающих 20 мг 1 раз/сут.
Также ривароксабан дозозависимо увеличивает АЧТВ и результат HepTest; однако эти параметры не рекомендуется использовать для оценки фармакодинамических эффектов ривароксабана.
В период лечения ривароксабаном проводить мониторинг параметров свертывания крови не требуется. Однако если для этого есть клиническое обоснование (например, при передозировке препарата или в случае необходимости экстренного хирургического вмешательства), концентрация ривароксабана может быть измерена при помощи калиброванного количественного теста анти-фактора Ха.
Фармакокинетика
Ривароксабан быстро всасывается; Cmax достигается через 2-4 ч после приема внутрь. Абсолютная биодоступность ривароксабана после приема в дозе 10 мг высокая (80-100%) независимо от приема пищи. При приеме ривароксабана в дозе 10 мг с пищей не отмечено изменения AUC и Cmax. Ривароксабан в дозе 10 мг можно назначать во время еды или независимо от приема пищи. Фармакокинетика ривароксабана характеризуется умеренной индивидуальной изменчивостью; индивидуальная изменчивость (вариационный коэффициент) составляет от 30% до 40%.
Всасывание ривароксабана зависит от места высвобождения в ЖКТ. В организме человека большая часть ривароксабана (92-95%) связывается с белками плазмы, основным связывающим компонентом является сывороточный альбумин. Vd — умеренный, Vss составляет приблизительно 50 л.
При приеме внутрь приблизительно 2/3 назначенной дозы ривароксабана подвергаются метаболизму и в дальнейшем выводятся равными частями с мочой и калом. Оставшаяся 1/3 дозы выводится посредством прямой почечной экскреции в неизмененном виде, главным образом, за счет активной почечной секреции.
Ривароксабан метаболизируется посредством изоферментов CYP3A4, CYP2J2, а также при помощи механизмов, независимых от системы цитохромов. Основными участками биотрансформации являются окисление морфолиновой группы и гидролиз амидных связей.
Ривароксабан является субстратом для белков-переносчиков P-gp (Р-гликопротеина) и BCRP (белка резистентности рака молочной железы).
Неизмененный ривароксабан является единственным активным соединением в человеческой плазме, значимые или активные циркулирующие метаболиты в плазме не обнаружены.
При выведении ривароксабана из плазмы конечный T1/2 составляет от 5 до 9 ч у молодых пациентов.
Ривароксабан, системный клиренс которого составляет приблизительно 10 л/ч, может быть отнесен к лекарственным веществам с низким уровнем клиренса.
Показания активных веществ препарата
Ксарелто®
Профилактика венозной тромбоэмболии (ВТЭ) у пациентов, подвергающихся большим ортопедическим оперативным вмешательствам на нижних конечностях.
Профилактика рецидивов тромбоза глубоких вен (ТГВ) или тромбоэмболии легочной артерии (ТЭЛА) после как минимум 6 месяцев лечения ТГВ или ТЭЛА.
Режим дозирования
Способ применения и режим дозирования конкретного препарата зависят от его формы выпуска и других факторов. Оптимальный режим дозирования определяет врач. Следует строго соблюдать соответствие используемой лекарственной формы конкретного препарата показаниям к применению и режиму дозирования.
Внутрь.
Рекомендуемая доза — 10-20 мг 1 раз/сут.
Частота и длительность применения устанавливаются индивидуально, в зависимости от показаний и клинической ситуации.
Побочное действие
Учитывая фармакологический механизм действия, применение ривароксабана может сопровождаться повышенным риском скрытого или явного кровотечения из любого органа или ткани, что может приводить к постгеморрагической анемии. Признаки, симптомы и степень тяжести (включая возможность летального исхода) будут отличаться в зависимости от локализации и степени тяжести или продолжительности кровотечения. Риск кровотечений может повышаться в определенных групп пациентов, например пациентов с неконтролируемой тяжелой артериальной гипертензией и/или у пациентов, принимающих препараты, оказывающие влияние на гемостаз. Геморрагические осложнения могут проявляться слабостью, астенией, бледностью, головокружением, головной болью или отеком неясной этиологии. Поэтому при оценке состояния пациента, получающего антикоагулянты, необходимо оценить вероятность возникновения кровотечения.
Со стороны крови и лимфатической системы: часто — анемия (включая соответствующие лабораторные показатели); нечасто — тромбоцитоз (включая повышение количества тромбоцитов).
Со стороны иммунной системы: нечасто — аллергическая реакция, аллергический дерматит.
Со стороны нервной системы: часто — головокружение, головная боль; нечасто — внутримозговые и внутричерепные кровоизлияния, обморок.
Со стороны сердечно-сосудистой системы: часто — снижение АД, гематома; нечасто — тахикардия.
Со стороны органа зрения: часто — кровоизлияние в глаз (включая кровоизлияние в конъюнктиву).
Со стороны дыхательной системы: часто — носовое кровотечение, кровохарканье.
Со стороны пищеварительной системы: часто — кровоточивость десен, желудочно-кишечное кровотечение (включая ректальное кровотечение), боли в области ЖКТ и в животе, диспепсия, тошнота, запор, диарея, рвота; нечасто — сухость во рту.
Со стороны печени и желчевыводящих путей: нечасто — нарушение функции печени: редко — желтуха.
Со стороны кожи и подкожных тканей: часто — кожный зуд (включая нечастые случаи генерализованного зуда), кожная сыпь, экхимоз, кожные и подкожные кровоизлияния; нечасто — крапивница.
Со стороны костно-мышечной системы и соединительной ткани: часто — боль в конечностях, гемартроз, кровоизлияние в мышцу.
Со стороны почек и мочевыводящих путей: часто — кровотечение из урогенитального тракта (включая гематурию), нарушение функции почек (включая повышение концентрации креатинина, повышение концентрации мочевины крови).
Со стороны половой системы: часто — кровотечение из урогенитального тракта (включая меноррагию).
Общие расстройства: лихорадка, периферические отеки, снижение общей мышечной силы и тонуса (включая слабость и астению); нечасто — ухудшение общего самочувствия (включая недомогание); редко — локальный отек.
Лабораторные и инструментальные данные: часто — повышение активности печеночных трансаминаз; нечасто — Повышение концентрации билирубина, повышение активности ЩФ, повышение активности ЛДГ, повышение активности липазы,
повышение активности амилазы, повышение активности ГГТ; редко — повышение концентрации
конъюгированного билирубина (при сопутствующем повышении активности АЛТ или без него.
Травмы, интоксикации и осложнения после манипуляций: часто — кровотечения после медицинской манипуляции (включая послеоперационную анемию и кровотечение из раны), гематома; нечасто — выделение секрета из раны; редко — сосудистая псевдоаневризма.
Противопоказания к применению
- повышенная чувствительность к ривароксабану;
- клинически значимые активные кровотечения (например, внутричерепные кровотечения, желудочно-кишечные кровотечения);
- повреждение или патологическое состояние, связанное с повышенным риском большого кровотечения (например, имеющаяся или недавно перенесенная желудочно-кишечная язва, наличие злокачественных новообразований с высоким риском кровотечения, недавние травмы головного или спинного мозга, недавние оперативные вмешательства на головном, спинном мозге или глазах, недавнее внутричерепное кровоизлияние, диагностированное или предполагаемое варикозное расширение вен пищевода, артериовенозные мальформации, аневризмы сосудов или большие аномалии строения сосудов головного или спинного мозга);
- сопутствующая терапия какими-либо другими антикоагулянтами, например, нефракционированным гепарином (НФГ), низкомолекулярными гепаринами (в т.ч. эноксапарин, далтепарину), производными гепарина (в т.ч. фондапаринукс), пероральными антикоагулянтами (в т.ч. варфарин, апиксабан, дабигатран), за исключением тех случаев, когда пациент переводится с терапии или на терапию ривароксабаном, или же когда НФГ назначается в низких дозах для поддержания проходимости центрального венозного или артериального катетера;
- заболевания печени, протекающие с коагулопатией, которая обусловливает клинически значимый риск кровотечения, включая пациентов с циррозом печени классов В и С по классификации Чайлд-Пью;
- тяжелая степень нарушения функции почек при КК<15 мл/мин (клинические данные о применении ривароксабана у пациентов данной категории отсутствуют);
- беременность;
- период грудного вскармливания;
- детский и подростковый возраст до 18 лет (эффективность и безопасность для пациентов данной возрастной группы не установлены).
С осторожностью
- при лечении пациентов с повышенным риском кровотечения (в т.ч. при врожденной или приобретенной склонности к кровотечениям, неконтролируемой тяжелой артериальной гипертензии, язвенной болезни желудка и двенадцатиперстной кишки в стадии обострения, недавно перенесенной язвенной болезни желудка и двенадцатиперстной кишки, сосудистой ретинопатии, недавно перенесенном внутричерепном или внутримозговом кровоизлиянии, при патологии сосудов спинного или головного мозга, после недавно перенесенной операции на головном, спинном мозге и глазах, бронхоэктазах или легочном кровотечении в анамнезе);
- при лечении пациентов со средней степенью нарушения функции почек (КК 30-49 мл/мин), получающих одновременно препараты, повышающие концентрацию ривароксабана в плазме крови (см. раздел «Лекарственное взаимодействие»);
- при лечении пациентов с тяжелой степенью нарушения функции почек (КК 15-29 мл/мин);
- ривароксабан не рекомендуется к применению у пациентов, получающих системное лечение противогрибковыми препаратами группы азолов (например, кетоконазолом) или ингибиторами протеазы ВИЧ (например, ритонавиром) (см. раздел «Лекарственное взаимодействие»);
- пациенты с тяжелой степенью нарушения функции почек (КК 15-29 мл/мин), повышенным риском кровотечения и пациенты, получающие сопутствующее системное лечение противогрибковыми препаратами группы азолов или ингибиторами протеазы ВИЧ, после начала лечения должны находиться под пристальным контролем для своевременного обнаружения осложнений в форме кровотечений. Такой контроль может включать регулярное физикальное обследование пациентов, тщательное наблюдение за отделяемым по дренажу хирургической раны и периодические измерения уровня гемоглобина. Любое понижение гемоглобина или АД, для которого нет объяснения, является основанием для поиска источника кровотечения;
- у пациентов, одновременно получающих лекарственные препараты, влияющие на гемостаз, например, НПВП, антиагреганты, другие антитромботические средства или селективные ингибиторы обратного захвата серотонина (СИОЗС) и селективные ингибиторы обратного захвата серотонина и норэпинефрина (СИОЗСН);
- у пациентов с риском обострения язвенной болезни желудка и двенадцатиперстной кишки может быть оправдано назначение профилактического противоязвенного лечения.
Применение при беременности и кормлении грудью
Противопоказано применение при беременности и в период грудного вскармливания.
Применение при нарушениях функции печени
Противопоказано применение препарата при заболеваниях печени, протекающих с коагулопатией, которая обусловливает клинически значимый риск кровотечения, включая пациентов с циррозом печени классов В и С по классификации Чайлд-Пью.
Для пациентов с тяжелой печеночной недостаточностью (класс С по классификации Чайлд-Пью) клинические данные отсутствуют.
Больным с другими заболеваниями печени изменения дозы не требуются.
Применение при нарушениях функции почек
Противопоказано применение препарата при лечении пациентов с тяжелой степенью нарушения функции почек при КК<15 мл/мин.
С осторожностью следует применять препарат при лечении пациентов со средней степенью нарушения функции почек (КК 30-49 мл/мин), получающих одновременно препараты, повышающие концентрацию ривароксабана в плазме крови; а также при лечении пациентов с тяжелой степенью нарушения функции почек (КК 15-29 мл/мин).
Применение у детей
Противопоказано применение в детском и подростковом возрасте до 18 лет.
Применение у пожилых пациентов
Коррекция дозы в зависимости от возраста больного (старше 65 лет) не требуется.
Особые указания
Применение сопутствующих препаратов
Применение ривароксабана не рекомендуется у пациентов, получающих сопутствующее системное лечение противогрибковыми препаратами группы азолов (например, кетоконазолом) или ингибиторами ВИЧ-протеазы (например, ритонавиром). Эти препараты являются сильными ингибиторами CYP3A4 и Р-гликопротеина. Таким образом, данные препараты могут повышать концентрацию ривароксабана в плазме крови до клинически значимых значений (в 2.6 раза в среднем), что может привести к повышенному риску кровотечений.
Однако противогрибковый препарат группы азолов флуконазол, умеренный ингибитор CYP3A4, оказывает менее выраженное действие на экспозицию ривароксабана и может применяться с ним одновременно.
Нарушение функции почек
Ривароксабан следует с осторожностью применять у пациентов со средней степенью нарушения функции почек (КК 30-49 мл/мин), получающих сопутствующие препараты, которые могут приводить к повышению концентрации ривароксабана в плазме. У пациентов с тяжелой степенью нарушения функции почек (КК<30 мл/мин) концентрация ривароксабана в плазме может быть значительно повышена (в 1.6 раза в среднем), что может привести к повышенному риску кровотечения. Вследствие основного заболевания у таких пациентов имеется повышенный риск развития как кровотечения, так и тромбоза. В связи с ограниченным количеством клинических данных, ривароксабан следует применять с осторожностью у пациентов с КК 15-29 мл/мин. Клинические данные о применении ривароксабана у пациентов с тяжелым нарушением функции почек (КК <15 мл/мин) отсутствуют. Поэтому применение ривароксабана у таких пациентов не рекомендуется.
За пациентами с тяжелым нарушением функции почек (КК 15-29 мл/мин) или повышенным риском кровотечения, а также пациентами, получающими сопутствующее системное лечение противогрибковыми препаратами группы азолов или ингибиторами ВИЧ-протеаз, необходимо проводить тщательное наблюдение на предмет наличия признаков кровотечения после начала лечения.
Наблюдение может осуществляться путем проведения регулярного физикального обследования пациентов, тщательного контроля за состоянием дренажа послеоперационной раны, а также путем периодического определения гемоглобина.
Оперативные вмешательства при переломе проксимальных отделов бедренной кости
Имеются ограниченные клинические данные, полученные в наблюдательных исследованиях, у пациентов, подвергающихся оперативным вмешательствам при переломе нижних конечностей, в т.ч. при переломе проксимальных отделов бедренной кости.
Риск кровотечения
Как и при приеме других антикоагулянтов необходимо тщательно наблюдать пациентов, принимающих ривароксабан, для выявления признаков кровотечения.
В случае тяжелого кровотечения прием ривароксабана следует прекратить.
В клинических исследованиях кровотечения из слизистых оболочек (а именно: кровотечение из носа, десен, ЖКТ, мочеполовой системы, включая аномальное вагинальное или усиленное менструальное кровотечение) и анемия наблюдались чаще при длительном лечении ривароксабаном по сравнению с лечением АВК. Таким образом, в дополнение к надлежащему клиническому наблюдению, лабораторное исследование гемоглобина/гематокрита может быть значимым для выявления скрытых кровотечений и количественной оценки клинической значимости явных кровотечений, которые будут сочтены допустимыми.
Ривароксабан, как и другие антитромботические средства, следует с осторожностью применять у пациентов, имеющих повышенный риск кровотечений, в т.ч. пациентов с врожденной или приобретенной склонностью к кровотечениям; пациентов с неконтролируемой тяжелой артериальной гипертензией; пациентов с язвенной болезнью желудка и двенадцатиперстной кишки в фазе обострения; пациентов, недавно перенесших язвенную болезнь желудка и двенадцатиперстной кишки; пациентов с сосудистой ретинопатией; пациентов, недавно перенесших внутричерепное или внутримозговое кровоизлияние; пациентов с патологией сосудов головного или спинного мозга; пациентов, недавно перенесших операцию на головном, спинном мозге или глазах; пациентов с бронхоэктазами или легочным кровотечением в анамнезе.
Следует соблюдать осторожность, если пациент одновременно получает лекарственные препараты, влияющие на гемостаз, такие как НПВП, ингибиторы агрегации тромбоцитов, другие антитромботические препараты или СИОЗС и СИОЗСН.
Пациентам с риском развития язвенной болезни желудка и двенадцатиперстной кишки может быть назначено соответствующее профилактическое лечение.
При необъяснимом снижении гемоглобина или АД необходимо искать источник кровотечения.
Терапия ривароксабаном не требует рутинного мониторинга его экспозиции. Тем не менее измерение концентрации ривароксабана с помощью калиброванного теста для количественного определения анти-Ха активности, может оказаться полезным в исключительных случаях, когда информация об экспозиции ривароксабана может быть использована при принятии клинически значимых решений, например, в случае передозировки или экстренного хирургического вмешательства.
Спинальная анестезия
При выполнении эпидуральной/спинальной анестезии или спинномозговой пункции у пациентов, получающих ингибиторы агрегации тромбоцитов с целью профилактики тромбоэмболических осложнений, существует риск развития эпидуральной или спинномозговой гематомы, которая может привести к длительному параличу. Риск этих событий в дальнейшем повышается при применении постоянного эпидурального катетера или сопутствующей терапии лекарственными препаратами, влияющими на гемостаз. Травматичное выполнение эпидуральной или спинномозговой пункции или повторная пункция также могут способствовать повышению риска.
Пациенты должны находиться под наблюдением для выявления признаков и симптомов неврологических нарушений (например, онемение или слабость ног, дисфункция кишечника или мочевого пузыря). При обнаружении неврологических расстройств необходима срочная диагностика и лечение.
Врач должен сопоставить потенциальную пользу и риск перед проведением спинномозгового вмешательства пациентам, получающим антикоагулянты или которым планируется назначение антикоагулянтов с целью профилактики тромбозов.
С целью снижения потенциального риска кровотечения, ассоциированного с одновременным применение ривароксабана и эпидуральной/спинальной анестезии или спинальной пункции, следует учитывать фармакокинетический профиль ривароксабана. Установку или удаление эпидурального катетера или люмбальную пункцию лучше проводить тогда, когда антикоагулянтный эффект ривароксабана оценивается как слабый.
Эпидуральный катетер извлекают не ранее чем через 18 ч после назначения последней дозы ривароксабана. Ривароксабан не следует назначать ранее чем через 6 ч после извлечения эпидурального катетера. В случае травматичной пункции применение ривароксабана следует отложить на 24 ч.
Хирургические операции и вмешательства
Если необходимо проведение инвазивной процедуры или хирургического вмешательства, прием ривароксабан следует прекратить, по крайней мере, за 24 ч до вмешательства, если это возможно, и на основании заключения врача. Если процедуру нельзя отложить, повышенный риск кровотечения следует оценивать в сравнении с необходимостью срочного вмешательства.
Прием ривароксабана следует возобновить после инвазивной процедуры или хирургического вмешательства при условии наличия соответствующих клинических показателей и адекватного гемостаза.
Женщины репродуктивного возраста
Ривароксабан можно принимать женщинам детородного возраста только при условии применения эффективных методов контрацепции.
Кожные реакции
При проведении постмаркетинговых наблюдений сообщалось о случаях возникновения синдрома Стивенса-Джонсона и токсического эпидермального некролиза. При первом появлении тяжелой кожной сыпи (например, при ее распространении, интенсификации и/или образовании волдырей) или при наличии других симптомов гиперчувствительности, связанных с поражением слизистой оболочки, следует прекратить терапию ривароксабаном.
Пациенты с искусственными клапанами сердца
Основываясь на данных рандомизированного контролируемого клинического исследования по сравнению терапии ривароксабаном и антитромбоцитарной терапии, применение ривароксабаном не рекомендуется для профилактики тромбозов у пациентов, перенесших недавнюю транскатетерную замену аортального клапана (TAVR). Безопасность и эффективность применения ривароксабана не изучались у пациентов с какими-либо другими искусственными клапанами сердца или у пациентов после иных вмешательств на клапанах сердца, следовательно, нет данных, подтверждающих, что применение ривароксабана обеспечивает достаточный антикоагулянтный эффект у данных категорий пациентов.
Пациенты с высоким риском тройного позитивного антифосфолипидного синдрома
Применение ривароксабана не рекомендуется у пациентов, имеющих тромбозы в анамнезе, у которых диагностирован устойчивый тройной позитивный антифосфолипидный синдром (наличие волчаночного антикоагулянта, антител к кардиолипину и антител к бета-2-гликопротеину I), поскольку терапия ривароксабаном сопровождается повышенной частотой рецидивов тромботических событий в сравнении с терапией АВК.
Пациенты с гемодинамически нестабильной ТЭЛА и пациенты, которым требуется проведение тромболизиса или тромбэктомии
Ривароксабан не рекомендуется в качестве альтернативы нефракционированному гепарину у пациентов с гемодинамически нестабильной тромбоэмболией легочной артерии, а также у пациентов, которые могут нуждаться в проведении тромболизиса или тромбэктомии, поскольку безопасность и эффективность ривароксабана при таких клинических ситуациях не установлена.
Данные по безопасности, полученные из доклинических исследований
За исключением эффектов, связанных с усилением фармакологического действия (кровотечений), при анализе доклинических данных, полученных в исследованиях по фармакологической безопасности, специфической опасности для человека не обнаружено.
Влияние на способность к управлению транспортными средствами и механизмами
При применении ривароксабана отмечались случаи обмороков и головокружения, которые могут влиять на способность управления транспортными средствами или другими механизмами. Пациентам, у которых возникают такие неблагоприятные реакции, не следует управлять транспортными средствами или другими механизмами.
Лекарственное взаимодействие
Выведение ривароксабана осуществляется главным образом посредством метаболизма в печени, опосредованного системой цитохрома Р450 (CYP3A4, CYP2J2), а также — путем почечной экскреции неизмененного лекарственного вещества с использованием систем переносчиков P-gp/BCRP (Р-гликопротеина/белка устойчивости к раку молочной железы).
Одновременное применение ривароксабана и мощных ингибиторов изофермента CYP3A4 и Р-гликопротеина может привести к снижению почечного и печеночного клиренса ривароксабана и, таким образом, значительно увеличить его системное воздействие.
Совместное применение ривароксабана и противогрибкового средства из группы азолов кетоконазола (400 мг 1 раз/сут), являющегося мощным ингибитором CYP3A4 и Р-гликопротеина, приводило к повышению средней равновесной AUC ривароксабана в 2.6 раза и увеличению средней Cmax ривароксабана в 1.7 раза, что сопровождалось значительным усилением фармакодинамического действия ривароксабана.
Совместное назначение ривароксабана и ингибитора протеазы ВИЧ ритонавира (600 мг 2 раза/сут), являющегося мощным ингибитором CYP3A4 и Р-гликопротеина, приводило к увеличению средней равновесной AUC ривароксабана в 2.5 раза и увеличению средней Cmax ривароксабана в 1.6 раза, что сопровождалось значительным усилением фармакодинамического действия ривароксабана. В связи с этим ривароксабан не рекомендуется к применению у пациентов, получающих системное лечение противогрибковыми препаратами группы азолов или ингибиторами протеазы ВИЧ.
Ожидается, что другие лекарственные вещества, сильно угнетающие только один из путей выведения ривароксабана – с участием CYP3A4 или Р-гликопротеина, будут увеличивать концентрацию ривароксабана в плазме до менее значимых значений.
Кларитромицин (500 мг 2 раза/сут), мощный ингибитор изофермента CYP3A4 и умеренный ингибитор Р-гликопротеина, вызывал увеличение значений AUC в 1.5 раза и Cmax ривароксабана в 1.4 раза. Это увеличение имеет порядок нормальной изменчивости AUC и Cmax и считается клинически незначимым.
Эритромицин (500 мг 3 раза/сут), умеренный ингибитор изофермента CYP3A4 и Р-гликопротеина, вызывал увеличение значений AUC и Cmax ривароксабана в 1.3 раза. Это увеличение имеет порядок нормальной изменчивости AUC и Cmax и считается клинически незначимым.
У пациентов с легкой степенью нарушения функции почек (КК 50-80 мл/мин) эритромицин (500 мг 3 раза/сут) вызывал увеличение значений AUC ривароксабана в 1.8 раза и Cmax в 1.6 раза по сравнению с пациентами с нормальной функцией почек, не получавших сопутствующей терапии. У пациентов со средней степенью нарушения функции почек (КК 30-49 мл/мин) эритромицин вызывал увеличение значений AUC ривароксабана в 2.0 раза и Cmax в 1.6 раза по сравнению с пациентами с нормальной функцией почек, не получавших сопутствующей терапии.
Флуконазол (400 мг 1 раз/сут), умеренный ингибитор изофермента CYP3A4, вызывал увеличение средней AUC ривароксабана в 1.4 раза и увеличение средней Cmax в 1.3 раза. Это увеличение имеет порядок нормальной изменчивости AUC и Cmax считается клинически незначимым.
Следует избегать одновременного применения ривароксабана с дронедароном в связи с ограниченностью клинических данных о совместном применении.
Совместное применение ривароксабана и рифампицина, являющегося мощным индуктором CYP3A4 и Р-гликопротеина, приводило к снижению средней AUC ривароксабана приблизительно на 50% и параллельному уменьшению его фармакодинамических эффектов. Совместное применение ривароксабана с другими мощными индукторами CYP3A4 (например, фенитоином, карбамазепином, фенобарбиталом или препаратами зверобоя продырявленного) также может привести к снижению концентрации ривароксабана в плазме. Уменьшение концентрации ривароксабана в плазме признано клинически незначимым. Мощные индукторы CYP3A4 необходимо применять с осторожностью.
После одновременного применения эноксапарина натрия (однократная доза 40 мг) и ривароксабана (однократная доза 10 мг) наблюдался суммированный эффект в отношении активности анти-фактора Ха, не сопровождавшийся дополнительными суммированными эффектами в отношении проб на свертываемость крови (протромбиновое время, АЧТВ). Эноксапарин не изменял фармакокинетику ривароксабана.
После совместного применения препарата ривароксабана в дозе 15 мг и напроксена в дозе 500 мг клинически значимого увеличения времени кровотечения не наблюдалось. Тем не менее, у отдельных лиц возможен более выраженный фармакодинамический ответ.
Не обнаружено фармакокинетического взаимодействия между ривароксабаном в дозе 15 мг и клопидогрелом (нагрузочная доза 300 мг с последующим назначением поддерживающей дозы 75 мг), но у части пациентов обнаружено значимое увеличение времени кровотечения, не коррелировавшее со степенью агрегации тромбоцитов и содержанием Р-селектина или GPIIb/IIIa-рецептора.
Перевод пациентов с варфарина (МНО от 2 до 3) на ривароксабан (20 мг) или с ривароксабана (20 мг) на варфарин (МНО от 2 до 3 ) сопровождался более чем аддитивным увеличением протромбинового времени/МНО (Неопластин) (в отдельных случаях до 12), тогда как эффекты изменения АЧТВ, подавления активности фактора Xa и эндогенного потенциала тромбина (ЭПТ) были аддитивными.
Для оценки фармакодинамических эффектов ривароксабана в переходный период можно провести анализ анти-Ха факторной активности, PiCT и HepTest, если на определяемые в их ходе показатели не повлиял варфарин.
Начиная с 4-го дня после отмены варфарина, все анализы (включая ПВ, АЧТВ, подавление активности фактора Xa и ЭПТ) отражали исключительно эффект препарата ривароксабана.
Для оценки фармакодинамических эффектов варфарина в переходный период можно использовать показатель МНО, измеренный в момент достижения Cmin ривароксабана (через 24 ч после приема дозы ривароксабана), т.к. в этот момент времени влияние ривароксабана на результаты анализа минимально.
Фармакокинетического взаимодействия между варфарином и ривароксабаном не обнаружено.
Лекарственное взаимодействие ривароксабана с АВК фениндионом не изучалось. Рекомендуется по мере возможности избегать перевода пациентов с терапии ривароксабаном на терапию АВК фениндионом и наоборот.
Имеется ограниченный опыт перевода пациентов с терапии АВК аценокумаролом на ривароксабан.
Если возникает необходимость перевести пациента с терапии ривароксабаном на терапию АВК фениндионом или аценокумаролом, то следует соблюдать особую осторожность, в период совместного приема ривароксабана и АВК ежедневный контроль фармакодинамического действия препаратов (МНО, протромбиновое время) должен проводиться непосредственно перед приемом следующей дозы ривароксабана.
Если возникает необходимость перевести пациента с терапии АВК фениндионом или аценокумаролом на терапию ривароксабана, то следует соблюдать особую осторожность, контроль фармакодинамического действия препаратов при этом не требуется.
Как и в случае применения других антикоагулянтов, необходимо соблюдать осторожность при совместном применении ривароксабана с селективными ингибиторами обратного захвата серотонина (СИОЗС) и селективными ингибиторами обратного захвата серотонина и норэпинефрина (СИОЗСН), поскольку применение этих препаратов повышает риск кровотечения. Результаты клинических исследований продемонстрировали численное повышение больших и небольших клинически значимых кровотечений во всех группах лечения при совместном применении этих препаратов.
Влияние на результаты проб на параметры свертывания (протромбиновое время, АЧТВ, HepTest) соответствует ожидаемому с учетом механизма действия ривароксабана.
Адрес производителя
|
BAYER , AG |
Германия |
Kaiser-Wilhelm-Allee, 51368 Leverkusen, Germany |
|
ПОЛИСАН НТФФ , ООО |
Россия |
192102, г. Санкт-Петербург, ул. Салова, д. 72, к. 2, лит. А |
Если вы хотите разместить ссылку на описание этого препарата — используйте данный код
Аналоги препарата
-
Зинакорен
(Химико-фармацевтический комбинат АКРИХИН, Россия) -
Ксилтесс®
(EGIS Pharmaceuticals, Венгрия) -
Ликвирел
(ГРОТЕКС, Россия) -
Риваксаб™
(MYLAN LABORATORIES, Индия) -
Риваксан-Нан
(АКАДЕМФАРМ, Республика Беларусь) -
Риваксоред®
(Dr. Reddy`s Laboratories, Индия) -
Ривароксабан — Вертекс
(ВЕРТЕКС, Россия)
Все аналоги
МНН: Ривароксабан
Производитель: Байер АГ
Анатомо-терапевтическо-химическая классификация: Ривароксабан
Номер регистрации в РК:
№ РК-ЛС-5№014326
Информация о регистрации в РК:
06.08.2019 — бессрочно
Информация о реестрах и регистрах
- русский
- қазақша
- Скачать инструкцию медикамента
Торговое наименование
Ксарелто
Международное непатентованное название
Ривароксабан
Лекарственная форма
Таблетки,
покрытые пленочной оболочкой, 10 мг
Фармакотерапевтическая группа
Кровь и органы
кроветворения.
Антитромботические препараты. Прямые
ингибиторы фактора Ха. Ривароксабан.
Код
АТХ В01AF01
Показания к применению
—
профилактика венозной тромбоэмболии (ВТЭ) у взрослых пациентов после
планового протезирования тазобедренного или коленного сустава
—
лечение тромбоза глубоких вен (ТГВ) и тромбоэмболии легочной артерии
(ТЭЛА), а также профилактика повторного ТГВ и ТЭЛА у взрослых.
Перечень
сведений, необходимых до начала применения
Противопоказания
-
повышенная
чувствительность к ривароксабану или вспомогательным веществам
препарата -
активное клинически
значимое кровотечение -
нарушение
или состояние,
считающееся
значимым фактором риска большого кровотечения,
такие как имеющаяся или недавно имевшая
место язва желудочно-кишечного тракта,
наличие злокачественных новообразований с
высоким риском кровотечения, недавняя травма головного или спинного
мозга, недавнее хирургическое вмешательство на головном, спинном
мозге или глазах, недавнее внутричерепное кровоизлияние,
диагностированное или подозрение на варикозное
расширение вен пищевода, артериовенозные
аномалии развития,
сосудистые аневризмы или патология крупных сосудов спинного или
головного мозга. -
сопутствующая терапия
любыми другими антикоагулянтами, такими как нефракционированный
гепарин (НФГ), низкомолекулярные гепарины (эноксапарин, далтепарин и
т.д.), производные гепарина (фондапаринукс и т.д.), пероральные
антикоагулянты (варфарин, дабигатрана этексилат, апиксабан и т.п.),
за исключением особых случаев перехода на другую антикоагулянтную
терапию или когда НФГ вводится в дозах, необходимых для обеспечения
проходимости центрального венозного или артериального катетера -
заболевание печени,
сопровождающееся коагулопатией, связанной с риском развития
клинически значимого кровотечения, включая пациентов с циррозом
печени класса В и С по Чайлд-Пью -
беременность и период
грудного вскармливания -
лица
с наследственной непереносимостью фруктозы, дефицитом фермента Lapp
— лактазы, мальабсорбцией глюкозы-галактозы.
Необходимые
меры предосторожности при применении
На
протяжении всего периода лечения
рекомендуется проводить клиническое
наблюдение в рамках установленной практики антикоагулятной терапии.
Риск
кровотечения
Как
и при применении других антикоагулянтов, на фоне приема
Ксарелто,
необходимо тщательно наблюдать за пациентами для
выявления признаков кровотечения. Рекомендуется
использовать Ксарелто
с осторожностью при лечении пациентов с повышенным риском
кровотечения. При развитии тяжелого кровотечения
прием Ксарелто®
должен быть прекращен.
Кровотечения
из слизистых оболочек (например, носовое, десневое,
желудочно-кишечное
и из
мочеполового
тракта,
включая патологическое
вагинальное и более обильное менструальное кровотечение)
и анемия часто отмечались при длительном лечении препаратом Ксарелто®
по сравнению с лечением АВК. Следовательно,
в дополнение к стандартному
клиническому наблюдению,
и, если целесообразно, может иметь ценность лабораторное
определение
уровня гемоглобина/гематокрита для выявления
скрытого кровотечения и
количественная оценка клинической значимости явного кровотечения.
Несколько
подгрупп пациентов, описанных ниже, имеют повышенный риск развития
кровотечения.
Эти
пациенты с момента начала лечения должны находиться под тщательным
наблюдением врача для выявления признаков и симптомов кровотечения и
анемии. Для пациентов, получающих Ксарелто
10 мг для профилактики венозной тромбоэмболии (ВТЭ) у взрослых
пациентов с запланированным протезированием тазобедренного или
коленного сустава это может обеспечиваться регулярным медицинским
осмотром, тщательным наблюдением за отделяемым операционной раны и
периодическим определением уровня гемоглобина. При необъяснимом
падении уровня гемоглобина или артериального давления необходимо
искать источник кровотечения.
Несмотря
на то, что лечение препаратом Ксарелто
не требует рутинного мониторинга экспозиции, в исключительных
ситуациях, когда знание об экспозиции ривароксабана может помочь в
принятии клинического решения, например, при передозировке и
экстренной операции, измерение ривароксабана с помощью калиброванного
количественного теста активности против Xa фактора может оказаться
полезным.
Почечная
недостаточность
У
больных с тяжелой почечной
недостаточностью (клиренс креатинина <30
мл/мин) концентрации ривароксабана в плазме крови могут быть
значительно повышены (в среднем в 1,6 раза), что может привести к
повышенному риску кровотечений.
Необходимо
с осторожностью применять Ксарелто®
при лечении больных с тяжелой почечной недостаточностью с клиренсом
креатинина 15-29 мл/мин. Применение Ксарелто
не рекомендуется у больных с клиренсом креатинина <15 мл/мин.
Необходимо
с осторожностью применять Ксарелто®
при лечении больных с умеренной почечной недостаточностью (клиренс
креатинина 30-49 мл/мин), получающих сопутствующее лечение другими
препаратами, повышающими концентрацию ривароксабана в плазме крови.
Взаимодействие
с другими лекарственными препаратами
Ксарелто®
не рекомендуется к применению у пациентов, получающих системное
лечение противогрибковыми препаратами азоловой группы (например,
кетоконазолом, итраконазолом, вориконазолом и позаконазолом) или
ингибиторами протеазы ВИЧ (например, ритонавиром). Эти лекарственные
препараты являются сильными ингибиторами CYP3A4
и гликопротеина Р. Как следствие, эти лекарственные препараты могут
повышать концентрацию ривароксабана в плазме до клинически значимого
уровня (в среднем в 2,6 раза), что увеличивает риск развития
кровотечений.
Необходимо
соблюдать осторожность при назначении Ксарелто
пациентам, получающим лекарственные препараты, влияющие на гемостаз,
например, нестероидные противовоспалительные средства (НПВС),
ацетилсалициловую кислоту (АСК) и ингибиторы агрегации тромбоцитов
или селективные
ингибиторы обратного захвата
серотонина (СИОЗС) и
ингибиторы обратного
захвата серотонина
и норэпинефрина
(СИОЗСН). Пациентам, имеющим риск развития
язвенной болезни желудочно-кишечного тракта, следует рассмотреть
вопрос о проведении соответствующего профилактического лечения.
Пациенты,
получающие лечение Ксарелто®
в сочетании с АСК или Ксарелто®
и АСК плюс клопидогрел/ тиклопидин,
должны получать длительную терапию НПВС только в случаях, когда
польза превышает имеющийся риск кровотечения.
Другие
факторы риска развития кровотечения
Ксарелто,
так же, как и другие антитромботические препараты, не рекомендуется
использовать при лечении пациентов с повышенным риском кровотечения,
а именно с такими состояниями как:
-
врожденные
или приобретенные
нарушения, связанные с
кровотечениями -
неконтролируемая
тяжелая артериальная гипертония -
другие
заболевания желудочно-кишечного тракта без
активного изъязвления, которые могут
осложняться кровотечениями (например, воспалительные заболевания
кишечника, эзофагит, гастрит, гастроэзофагеальный рефлюкс) -
сосудистая
ретинопатия -
бронхоэктазы
или легочное кровотечение в анамнезе
Пациенты
с искусственным клапаном сердца
Ксарелто®
не следует использовать для тромбопрофилактики у пациентов, недавно
перенесших транскатетерную замену аортального клапана (TAVR).
Безопасность и эффективность применения Ксарелто®
у пациентов с искусственным клапаном сердца не изучалась,
следовательно, данные об адекватном антикоагулянтном действии
Ксарелто®
у такой популяции пациентов отсутствуют. Не рекомендуется лечение
препаратом Ксарелто®
у таких пациентов.
Пациенты
с антифосфолипидным синдромом (АФС).
Пациентам, с тромбозом в анамнезе, у
которых диагностирован антифосфолипидный синдром, не рекомендуется
назначать пероральные антикоагулянты прямого действия, включая
ривароксабан. Лечение пероральными антикоагулянтами прямого действия
может быть связано с повышением частоты рецидивирующих тромботических
событий по сравнению с терапией антагонистами витамина К, в
особенности у пациентов с позитивностью всех трех типов
антифосфолипидных антител (волчаночный антикоагулянт, антитела к
кардиолипину и антитела к бета-2-гликопротеину -1).
Хирургические
вмешательства при переломах бедренной кости
Оценка эффективности и безопасности
ривароксабана не изучалась во время
интервенционных клинических исследований с участием пациентов,
которым проводятся хирургические вмешательства при переломах
бедренной кости.
Гемодинамически
нестабильные пациенты с ТЭЛА, нуждающиеся в тромболизисе или легочной
эмболэктомии
Ксарелто®
не рекомендуется применять в качестве альтернативы
нефракционированного гепарина у пациентов с ТЭЛА и нестабильностью
гемодинамики или у которых возможно проведение тромболизиса или
легочной эмболэктомии, поскольку безопасность и эффективность
Ксарелто®
при данных клинических ситуациях не была установлена.
Нейроаксиальная
(эпидуральная/спинальная) анестезия
При
проведении нейроаксиальной (спинальной/эпидуральной)
анестезии или спинальной/эпидуральной
пункции, пациенты, принимающие
антитромботические средства для профилактики тромбоэмболических
осложнений, подвергаются риску развития эпидуральной или спинальной
гематомы, которая может вызвать длительный или стойкий паралич.
Риск
развития таких явлений повышается еще больше при использовании
постоянных эпидуральных катетеров или при совместном приеме
препаратов, влияющих на гемостаз. Риск может так же повышаться после
травматичной или повторной
эпидуральной или спинальной пункции. Пациентов следует часто
контролировать для выявления признаков или симптомов неврологических
нарушений (например, онемение или слабость в ногах, дисфункция
толстого кишечника или мочевого пузыря). При обнаружении
неврологических отклонений необходимо провести срочную диагностику и
лечение пациента. Врач должен учитывать потенциальную пользу по
отношению к риску, прежде чем проводить нейроаксиальное вмешательство
у пациентов, получающих антикоагулянты или пациентов, которым
предстоит антикоагулянтная терапия для тромбопрофилактики.
С
целью снижения потенциального риска кровотечения, ассоциированного с
проведением эпидуральной/спинальной анестезии и или спинальной
пункции на фоне одновременного применения ривароксабана, следует
учитывать фармакокинетический профиль ривароксабана. Установку или
удаление эпидурального катетера или люмбальную пункцию лучше
проводить тогда, когда антикоагулянтный эффект ривароксабана
оценивается как слабый.
Эпидуральный
катетер извлекают не ранее чем через 18 часов после назначения
последней дозы Ксарелто®.
Ксарелто® не
следует назначать ранее, чем через 6 часов после извлечения
эпидурального катетера.
В
случае травматической пункции назначение Ксарелто®
следует отложить на 24 часа.
Рекомендации
по дозировке при инвазивных процедурах и хирургических
вмешательствах, кроме планового
эндопротезирования тазобедренного или коленного сустава
Если
требуется проведение инвазивной процедуры или хирургического
вмешательства, прием Ксарелто®
10 мг следует, по возможности прекратить, по крайней мере, за 24 часа
до вмешательства и на основании клинического заключения врача.
Если
процедуру нельзя отложить, повышенный риск кровотечения следует
оценивать в сопоставлении со срочностью вмешательства.
Прием
Ксарелто®
следует возобновить как можно скорее после инвазивной процедуры или
хирургического вмешательства, если по оценке лечащего врача позволяет
клиническая ситуация и достигнут адекватный гемостаз.
Пожилые
пациенты
С
увеличением возраста пациента возрастает риск развития кровотечения.
Кожные
реакции
Серьезные кожные реакции, включая синдром
Стивенса-Джонсона/токсический эпидермальный некролиз и DRESS-синдром,
сообщались в ходе постмаркетингового наблюдения во временной
взаимосвязи с применением ривароксабана. По-видимому, наиболее
высокий риск проявления таких реакций у пациентов приходится на
начало лечения: в большинстве случаев такие реакции проявляются в
течение первых недель лечения. При появлении первых признаков тяжелой
кожной сыпи (т.е. распространение, усиление сыпи и/или образование
волдырей) или любых признаков гиперчувствительности со стороны
слизистых оболочек прием ривароксабана следует отменить.
Информация
о вспомогательных веществах
Препарат
Ксарелто®
содержит лактозу. Пациенты с редкими
наследственными проблемами непереносимости галактозы, Lapp
дефицит лактазы или глюкозо — галактозная мальабсорбция не должны
принимать этот лекарственный препарат.
Взаимодействия
с другими лекарственными препаратами
Взаимодействие
с ингибиторами CYP3A4
и гликопротеина
Р
Совместное
применение Ксарелто
и кетоконазола (400 мг 1 раз в сутки) или ритонавира (600 мг два раза
в сутки) приводило к повышению средней равновесной AUC
Ксарелто
в 2,6/2,5 раза и увеличению средней Смакс
Ксарелто®
в 1,7/1,6 раза, сопровождающимся значимым
усилением фармакодинамических эффектов препарата, способных привести
к повышенному риску развития кровотечений. Cледовательно,
применение Ксарелто®
не рекомендуется пациентам, получающим системную терапию азоловыми
противогрибковыми препаратами, такими как кетоконазол, итраконазол,
вориконазол и позаконазол, или ингибиторами протеазы ВИЧ. Эти
вещества являются сильными ингибиторами CYP3A4
и гликопротеина Р.
Ожидается,
что лекарственные вещества, сильно угнетающие только один из путей
выведения ривароксабана – с участием CYP3A4
или гликопротеина Р – в меньшей степени будут повышать
концентрацию ривароксабана в плазме.
К
примеру, кларитромицин (500 мг 2 раза в сутки), который считается
сильным ингибитором CYP3A4
и умеренным ингибитором гликопротеина Р, вызывал увеличение средней
AUC
в 1,5 раза и Смакс.
ривароксабана в 1,4 раза. Взаимодействие с кларитромицином, вероятно,
не является клинически значимым у большинства пациентов, но может
быть потенциально значимым у пациентов высокого риска.
Эритромицин
(500 мг 3 раза в сутки), умеренно подавляющий CYP3A4
и гликопротеин Р, вызывал увеличение средней AUC
и Смакс
ривароксабана в 1,3 раза. Взаимодействие с эритромицином, вероятно,
не является клинически значимым у большинства пациентов, но может
быть потенциально значимым у пациентов высокого риска.
У
пациентов с легкой почечной недостаточностью прием эритромицина (500
мг три раза в сутки) вызывал повышение средней
AUC
ривароксабана в 1,8 раз и Смакс.
в 1,6 раз по сравнению с лицами с нормальной функцией почек.
У
пациентов с умеренной почечной недостаточностью применение
эритромицина вызывало повышение средней
AUC
в 2,0 раза и Смакс
в 1,6 раз по сравнению с пациентами с нормальной функцией почек.
Эффект эритромицина
дополняет влияние
почечной недостаточности.
Флуконазол
(400 мг один раз в сутки),
считающийся умеренным ингибитором CYP3A4,
приводит к увеличению средней AUC
ривароксабана в 1,4 раза и увеличение средней Cmax
в 1,3 раза. Взаимодействие с флуконазолом, вероятно, не является
клинически значимым у большинства пациентов, но может быть
потенциально значимым у пациентов высокого риска.
Имеющиеся
клинические данные по применению дронедарона ограничены, поэтому
следует избегать его совместного применения с Ксарелто®.
Антикоагулянты
После
комбинированного применения эноксапарина (однократной дозы 40 мг) и
Ксарелто®
(однократной дозы 10 мг) наблюдалось
усиление
действия
против Ха
фактора, что не сопровождалось
дополнительными изменениями тестов
на свертываемость крови (протромбиновое время, АЧТВ). Эноксапарин не
влиял на фармакокинетику ривароксабана.
В
связи с повышенным риском кровотечений пациентам следует соблюдать
осторожность при применении Ксарелто®
совместно с другими антикоагулянтами.
Нестероидные
противовоспалительные средства (НПВС) / ингибиторы агрегации
тромбоцитов
После
совместного назначения Ксарелто®
(15 мг) и напроксена в дозе 500 мг клинически значимого удлинения
времени кровотечения не наблюдалось. Тем не менее, у отдельных лиц
возможен более выраженный фармакодинамический ответ.
При
совместном применении Ксарелто®
и ацетилсалициловой кислоты в дозе 500 мг клинически значимых
фармакокинетических и фармакодинамических взаимодействий не
наблюдалось.
Не
обнаружено фармакокинетического взаимодействия между Ксарелто®
15 мг и клопидогрелом (ударная доза 300 мг, затем поддерживающая доза
75 мг), однако у некоторых пациентов было обнаружено значимое
увеличение времени кровотечения, не коррелировавшее с агрегацией
тромбоцитов и уровнем Р-селектина или уровнем
рецепторов к GPIIb/IIIa.
Следует
соблюдать осторожность при одновременном назначении НВПС (включая
ацетилсалициловую кислоту) и ингибиторов агрегации тромбоцитов,
поскольку данные препараты, как правило, повышают риск кровотечения.
Селективный
ингибитор обратного захвата серотонина/серотонина-норэпинефрина
(СИОЗС/СИОЗСН)
Как
и в случае с другими антикоагулянтами, существует вероятность того,
что пациенты подвергаются повышенному риску кровотечения в случае
сочетанного применения с СИОЗС или СИОЗСН из-за их влияния на
тромбоциты. При одновременном использовании в клинической программе
ривароксабана во всех группах лечения отмечена более высокая частота
больших и небольших клинически значимых кровотечений.
Варфарин
Переход
пациентов с антагониста витамина К варфарина (МНО от 2,0 до 3,0) на
Ксарелто® (20
мг) или с Ксарелто®
(20 мг) на варфарин увеличивал протромбиновое время/МНО (реагент
Неопластин) в большей степени, чем этого можно было бы ожидать при
простом суммировании эффектов (отдельные значения МНО могут достигать
12), в то время как влияние на АЧТВ, подавление активности Ха фактора
и эндогенного потенциала тромбина было аддитивным.
В
случае необходимости исследования фармакодинамических эффектов
ривароксабана
во время такого переходного периода, в качестве необходимых тестов,
на которые не оказывает влияние варфарин, можно использовать
определение активности против
Ха
фактора, PiCT
и HepTest.
Начиная
с 4-го дня после отмены варфарина, все результаты анализов (в том
числе ПВ, АЧТВ, ингибирование активности Ха фактора и ЭПТ (эндогенный
потенциал тромбина)) отражают только эффект Ксарелто®.
В
случае необходимости исследования фармакодинамических эффектов
варфарина во время переходного
периода можно использовать определение МНО
на фоне C0
ривароксабана (через 24 часа после приема
предыдущей дозы Ксарелто®),
поскольку ривароксабан оказывает минимальное
влияние на этот показатель в данный период. Между
варфарином и Ксарелто®
не отмечено фармакокинетических взаимодействий.
Индукторы
CYP3A4
Совместное
назначение Ксарелто®
и сильного индуктора CYP3A4
рифампицина приводило к снижению средней AUC
ривароксабана приблизительно на 50% и параллельному уменьшению его
фармакодинамических эффектов. Совместное применение Ксарелто®
с другими сильными индукторами CYP3A4
(например, фенитоином, карбамазепином, фенобарбиталом или зверобоем
продырявленным) так же может привести к снижению концентраций
ривароксабана в плазме.
Поэтому
следует избегать назначения Ксарелто®
совместно с сильными индукторами CYP3A4
без тщательного наблюдения пациента в отношении признаков и симптомов
тромбоза.
Другое сопутствующее лечение
Не
отмечалось клинически значимых фармакокинетических или
фармакодинамических взаимодействий между ривароксабаном и мидазоламом
(субстрат CYP3A4),
дигоксином (субстрат гликопротеина Р) или аторвастатином (субстрат
CYP3A4
и гликопротеина Р) или омепразолом (ингибитор протонной помпы).
Ксарелто® не
ингибирует и не индуцирует основные изоферменты цитохрома CYP,
такие как CYP3A4.
Клинически
значимого взаимодействия Ксарелто®
с пищей не наблюдалось.
Лабораторные
параметры
Ожидается,
что Ксарелто®
влияет на параметры свертываемости крови (ПВ, АЧТВ, HepTest)
благодаря его механизму действия.
Специальные
предупреждения
Во
время беременности или лактации
Безопасность
и эффективность Ксарелто®
при лечении беременных женщин не установлены. Учитывая
потенциальную репродуктивную токсичность, риск кровотечения и
доказательства прохождения ривароксабана через гематоплацентарный
барьер, беременным женщинам ривароксабан противопоказан.
Женщинам репродуктивного возраста следует
избегать наступления беременности в период лечения препаратом
Ксарелто®
(следует использовать эффективные методы контрацепции в период
лечения Ксарелто®).
Безопасность
и эффективность Ксарелто®
у женщин в период грудного вскармливания не установлены. Ривароксабан
противопоказан во время кормления грудью. Должно
быть принято решение о прерывании грудного вскармливании либо о
прекращении/воздержании от лечения.
Фертильность
Специальные
исследования ривароксабана у людей для оценки влияния на фертильность
не проводились. .
Особенности
влияния препарата на способность управлять транспортным средством или
потенциально опасными механизмами
Ксарелто®
имеет незначительное влияние на способность управлять автотранспортом
и механизмами. Сообщалось
о случаях головокружения или обморочного состояния. Пациентам, у
которых наблюдались подобные реакции, следует воздержаться от
управления автотранспортом или механизмами.
Рекомендации
по применению
Режим
дозирования
Для
приема внутрь
Ксарелто®
можно принимать независимо от приема пищи.
Таблетки
Ксарелто® не
следует делить с целью приема сниженной дозы.
Для
пациентов, которые не могут проглотить таблетки целиком, таблетку
Ксарелто®
можно раздробить и смешать с водой или легкой пищей, такой как
яблочное пюре, непосредственно перед приемом и принимать перорально.
Раздробленную
таблетку Ксарелто®
можно вводить через желудочный зонд. Перед применением Ксарелто®
следует подтвердить наличие зонда в желудке. Раздробленную таблетку
следует вводить вместе с небольшим количеством воды через желудочный
зонд, после чего его необходимо промыть водой.
Дозировка
Профилактика
венозной тромбоэмболии (ВТЭ) у взрослых пациентов после планового
протезирования тазобедренного или коленного сустава
Рекомендуемая
доза препарата составляет 1 таблетка Ксарелто
10 мг 1 раз в сутки. Первую дозу следует принять
через 6-10 часов после операции, при условии достигнутого гемостаза.
Продолжительность
лечения определяется типом большой ортопедической операции и зависит
от индивидуального риска развития ВТЭ у пациента.
—
После большой операции на тазобедренном суставе рекомендованная
продолжительность лечения составляет 5 недель.
—
После большой операции на коленном суставе рекомендованная
продолжительность лечения составляет 2 недели.
В
случае пропуска дозы пациенту следует немедленно принять таблетку
Ксарелто
и на следующий день продолжить прием 1 раз в сутки, как до пропуска
дозы.
Лечение
тромбоза глубоких вен (ТГВ) и тромбоэмболии легочной артерии (ТЭЛА),
а также профилактика повторного ТГВ и ТЭЛА у взрослых
Рекомендованная
доза Ксарелто® для
начального лечения острого ТГВ или ТЭЛА составляет 15 мг два
раза в сутки в течение первых 3 недель, с
последующим приемом Ксарелто®
20 мг один раз в сутки
для продолжения терапии и профилактики повторного ТГВ и ТЭЛА.
Кратковременную
терапию (минимум 3 месяца) следует рассмотреть у пациентов с ТГВ и
ТЭЛА, спровоцированными большими транзиторными факторами риска
(например, недавние обширные оперативные вмешательства или травма).
Более длительную терапию следует рассмотреть у пациентов со
спровоцированными ТГВ или ТЭЛА, не связанными с большими
транзиторными факторами риска, с неспровоцированными ТГВ или ТЭЛА или
наличием в анамнезе рецидива ТГВ или ТЭЛА.
При
наличии показаний к продленной профилактике рецидива ТГВ и ТЭЛА
(после лечения ТГВ или ТЭЛА в течение как минимум 6 месяцев)
рекомендованная доза составляет 10 мг один раз в сутки. Пациенты с
высоким риском рецидива ТГВ или ТЭЛА, таким
как наличие осложненных сопутствующих заболеваний или рецидив ТГВ или
ТЭЛА на фоне продленной терапии Ксарелто®
в профилактической дозе 10 мг один раз в
сутки, следует рассмотреть прием дозы Ксарелто®
20 мг один раз в сутки.
Продолжительность
лечения и доза должны подбираться индивидуально – после
тщательной оценки пользы лечения по отношению к риску кровотечения.
|
Длительность |
Режим дозирования |
Общая суточная |
|
|
Лечение и |
С 1 по 21 дни |
15 мг два раза в |
30 мг |
|
С 22 дня и далее |
20 мг один раз в |
20 мг |
|
|
Профилактика |
После завершения |
10 мг один раз в сутки или 20 мг один раз в сутки |
10 мг или 20 мг |
Если
прием очередной дозы пропущен при приеме дозы 15 мг два раза в сутки
(1-21 дни лечения), пациент должен немедленно принять Ксарелто®
для того, чтобы обеспечить поступление суточной дозы 30 мг. Для этого
можно принять одновременно 2 таблетки Ксарелто®
в дозе 15 мг. На следующий день следует продолжить регулярный прием
препарата в дозе 15 мг 2 раза в сутки в соответствии с
рекомендованным режимом.
В
случае пропуска дозы при приеме препарата 1 раз в сутки пациенту
следует немедленно принять Ксарелто
и на следующий день продолжить лечение приемом 1 раз в сутки в
соответствии с рекомендованным режимом.
Не
следует удваивать принимаемую дозу для компенсации, пропущенной ранее
дозы.
Переход
с антагонистов витамина K (АВК) на Ксарелто®
У
пациентов на лечении ТГВ и ТЭЛА и на профилактике рецидива ТГВ и ТЭЛА
прием АВК следует прекратить, и по достижению МНО до ≤2,5 следует
начать лечение Ксарелто®.
При
переходе пациентов с АВК на Ксарелто®,
после приема Ксарелто® значения
МНО будут ложно повышенными. МНО не подходит для определения
антикоагулянтной активности Ксарелто®,
и поэтому не должно использоваться с этой целью.
Переход
с Ксарелто®
на антагонисты витамина К (АВК)
Существует
вероятность недостаточного антикоагулянтного эффекта при переходе с
Ксарелто® на
АВК. В связи с этим необходимо обеспечить непрерывный достаточный
антикоагулянтный эффект во время любого перехода на другой
антикоагулянт. Следует отметить, что Ксарелто®
может способствовать повышению МНО.
При
переходе с Ксарелто®
на АВК, Ксарелто® следует
принимать одновременно с АВК до тех пор, пока МНО не достигнет
показателя ≥2,0.
В
течение первых двух дней переходного периода следует применять
стандартную начальную дозу АВК с последующим назначением дозы АВК на
основании определений МНО. Во время одновременного приема Ксарелто®
и АВК, МНО следует определять не ранее чем через 24 часа после приема
предыдущей дозы и перед приемом следующей дозы Ксарелто®.
После прекращения применения Ксарелто®
достоверное определение МНО можно проводить минимум через 24 часа
после приема последней дозы препарата.
Переход
с парентеральных антикоагулянтов на Ксарелто®
Для
пациентов, получающих парентеральные антикоагулянты, следует отменить
парентеральный антикоагулянт, Ксарелто®
следует принимать за 0-2 часа до момента следующего планового
введения парентерального препарата (например, низкомолекулярного
гепарина) или в момент прекращения непрерывного введения
парентерального препарата (например, внутривенного введения
нефракционированного гепарина).
Переход
с Ксарелто®
на парентеральные антикоагулянты
Ввести
первую дозу парентерального антикоагулянта в момент, когда должна
была быть принята следующая доза Ксарелто®.
Дополнительная
информация по отдельным популяциям пациентов
Почечная
недостаточность
Данные
о применении Ксарелто
у больных с тяжелой почечной недостаточностью (клиренс креатинина
15-29 мл/мин) указывают на значительное повышение уровней
ривароксабана в плазме. В этой связи необходимо с осторожностью
применять Ксарелто®
в этой группе больных. Применение Ксарелто
не рекомендуется у больных с клиренсом креатинина <15 мл/мин.
—
Для профилактики венозной тромбоэмболии (ВТЭ) у взрослых пациентов с
плановым протезированием тазобедренного или коленного сустава не
требуется коррекция дозы Ксарелто
у больных с легкой почечной недостаточностью с клиренсом креатинина
50-80 мл/мин или умеренной почечной недостаточностью с клиренсом
креатинина 30-49 мл/мин).
—
Для лечения тромбоза глубоких вен (ТГВ) и тромбоэмболии легочной
артерии (ТЭЛА), а также профилактики повторного ТГВ и ТЭЛА не
требуется коррекция дозы Ксарелто
у больных с легкой почечной недостаточностью с клиренсом креатинина
50-80 мл/мин.
При умеренной почечной недостаточности
(клиренс креатинина 30-49 мл/мин) или с тяжелой почечной
недостаточности (клиренс креатинина 15-29 мл/мин) пациенты должны
принимать 15 мг два раза в сутки в течение первых 3 недель. Затем
рекомендованная доза составляет 20 мг один раз в сутки. Снижение дозы
с 20 мг один раз в сутки до 15 мг один раз в сутки следует
рассматривать, когда оцениваемый риск кровотечения у пациента
преобладает над риском повторного ТГВ и ТЭЛА. Рекомендация
использования 15 мг один раз в сутки основана на фармакокинетическом
моделировании и не изучена в клинических условиях при данном
состоянии.
При
рекомендованной ежедневной дозе препарата 10 мг 1 раз в сутки не
требуется коррекция дозы Ксарелто.
Печеночная
недостаточность
Применение
Ксарелто
противопоказано у больных с заболеваниями печени, сопровождающимися
коагулопатией и риском развития клинически значимого кровотечения,
включая цирроз печени класса B и C по
классификации Чайлд-Пью.
Пожилые
пациенты
Не
требуется коррекции дозы.
Масса
тела
Не
требуется коррекции дозы.
Пол
Не
требуется коррекции дозы.
Дети
и подростки
Безопасность
и эффективность Ксарелто
у детей и подростков младше 18 лет не установлены. Доступные данные
отсутствуют. Поэтому Ксарелто
не рекомендуется к применению у детей и подростков до 18 лет.
Меры,
которые необходимо принять в случае передозировки
Были
зарегистрированы редкие случаи передозировки при приеме ривароксабана
до 600 мг без развития кровотечений или других неблагоприятных
реакций. В связи с ограниченным всасыванием ожидается развитие
низкоуровневого плато концентрации препарата без дальнейшего
увеличения его экспозиции в плазме крови при применении доз,
превышающих терапевтические, равных 50 мг и выше.
Андексанет
альфа является специфическим антидотом (или препаратом обратного
действия), нейтрализующим
фармакодинамические
эффекты
ривароксабана (см. информацию в общей характеристике лекарственного
средства на андексанет альфа).
В
случае передозировки для снижения всасывания ривароксабана можно
использовать активированный уголь.
Тактика
при кровотечениях
Если
у пациента, получающего ривароксабан, возникло осложнение в виде
кровотечения, следующий прием препарата следует отложить или, при
необходимости, отменить. Период полувыведения ривароксабана
составляет приблизительно 5-13 часов. Лечение должно быть
индивидуальным в зависимости от тяжести и локализации кровотечения.
При необходимости можно использовать соответствующее симптоматическое
лечение, такое как механическая компрессия (например, при тяжелых
носовых кровотечениях), хирургический гемостаз с процедурами для
остановки кровотечения, восполнение жидкости и гемодинамическую
поддержку, переливание препаратов крови (эритроцитарной массы или
свежезамороженной плазмы, в зависимости от наличия сопутствующей
анемии или коагулопатии) или тромбоцитов.
Если
перечисленные выше мероприятия не приводят к устранению кровотечения,
следует рассмотреть назначение специфического препарата обратного
действия, ингибирующего действие Ха фактора
(андексанет альфа), который нейтрализует
фармакодинамические
эффекты
ривароксабана или назначение
специфических
прокоагулянтных
препаратов
обратного действия, таких,
как концентрат протромбинового комплекса
(КПК), концентрат активированного протромбинового комплекса (КАПК)
или рекомбинантный VIIa
фактор (рФVIIa).
Однако в настоящее время опыт применения данных препаратов у
пациентов, получающих Ксарелто®,
ограничен. Рекомендация также основана на ограниченных неклинических
данных. Повторное введение рФVIIa и титрование должно быть
рассмотрено в зависимости от положительной динамики кровотечения. В
зависимости от доступности на местном уровне в случае большого
кровотечения следует решить вопрос о консультации
специалиста-коагулолога.
Ожидаемо,
протамина сульфат и витамин К не будут оказывать влияние на
противосвертывающую активность Ксарелто®.
Имеется
ограниченный опыт применения транексамовой кислоты, и нет опыта
применения аминокапроновой кислоты и апротинина у пациентов,
получающих Ксарелто®.
Научное
обоснование целесообразности или опыт использования системных
гемостатических препаратов, таких как десмопрессин, у пациентов,
получающих Ксарелто®,
отсутствует. Учитывая интенсивное
связывание с белками плазмы крови, ожидается, что ривароксабан не
будет выводиться при проведении диализа.
Описание нежелательных реакций, которые
проявляются при стандартном применении ЛП и меры, которые следует
принять в этом случае
Обобщенные данные о частоте нежелательных
реакций, зарегистрированных при использовании Ксарелто®,
приведены ниже по классам систем органов (MedDRA) и частоте.
Нежелательные
реакции распределены в группы по частоте следующим образом:
очень
часто (≥1/10)
часто
(от ≥1/100 до <1/10)
нечасто
(от ≥ 1/1000 до <1/100)
редко
(от ≥ 1/10000 до <1/1000)
очень
редко (<1/10000)
с
неизвестной частотой (частота не может быть установлена по имеющимся
данным)
Все
возникшие на фоне лечения нежелательные реакции, зарегистрированные у
пациентов в ходе клинических исследований III фазы или
постмаркетингового применения
Часто
-
анемия (включая
соответствующие лабораторные показатели) -
головокружение,
головная боль -
кровоизлияние в глаз
(включая кровоизлияние в конъюнктиву) -
артериальная
гипотензия, гематома -
эпистаксис (носовое
кровотечение), кровохаркание -
кровоточивость десен,
желудочно-кишечное кровотечение (включая ректальное кровотечение),
боли в области желудочно-кишечного тракта, диспепсия, тошнота, запор
А, диарея, рвота
А -
повышение уровня
трансаминаз -
зуд (включая нечастые
случаи генерализованного зуда), сыпь, экхимоз,
кожные и подкожные кровоизлияния -
боль в конечностях
А -
кровотечение из
урогенитального тракта (включая гематурию и меноррагию
B),
почечная недостаточность (включая повышение
концентрации креатинина, повышение концентрации мочевины) -
лихорадка (повышение
температуры) А,
периферические отеки, снижение общей мышечной
силы и тонуса (включая слабость и астению) -
кровоизлияния после
проведенных процедур (включая послеоперационную анемию и
кровотечение из раны), кровоподтек, выделения из
раны A
Нечасто
-
тромбоцитоз (включая
увеличение количества тромбоцитов) А,
тромбоцитопения -
аллергическая реакция,
аллергический дерматит, ангионевротический
отек и аллергический отек -
внутримозговое и
внутричерепное кровоизлияние, обморок -
тахикардия
-
сухость во рту
-
нарушение функции
печени, повышение уровней билирубина, щелочной фосфатазыА,
гамма-глютамилтрансферазы (ГГТ) А
в крови -
крапивница
-
гемартроз
-
ухудшение общего
самочувствия (включая недомогание) -
повышенный уровень ЛДГ
А, повышенный уровень липазы
А, повышенный уровень амилазы
А
Редко
-
желтуха, повышение
уровня конъюгированного билирубина (при сопутствующем повышении
аланинаминотрасферазы (АЛТ) или без него), холестаз, гепатит
(включая гепатоцеллюлярное повреждение) -
кровоизлияние в мышцы
-
местный отек А
-
сосудистая
псевдоаневризма С
Очень
редко
-
анафилактические
реакции, включая анафилактический шок -
синдром
Стивенса-Джонсона/токсический эпидермальный некролиз, DRESS-синдром
С
неизвестной частотой
-
компартмент- синдром
вследствие кровотечения -
почечная
недостаточность/ -
острая почечная
недостаточность вследствие кровотечения, достаточного для развития
гипоперфузии.
А:
регистрировались при
профилактике венозной тромбоэмболии (ВТЭ) у взрослых пациентов
после планового
протезирования коленного или тазобедренного сустава
B:
регистрировались при
лечении ТГВ и ТЭЛА и
профилактике рецидивов как очень частые у женщин < 55 лет
C:
регистрировались как
нечастые при профилактике внезапной смерти и инфаркта миокарда у
пациентов после острого коронарного синдрома (после проведения
чрескожных вмешательств).
Описание
некоторых нежелательных реакций
Учитывая
фармакологический механизм действия Ксарелто®,
применение его может сопровождаться повышенным риском скрытого или
явного кровотечения из любых органов и тканей, которое может
приводить к постгеморрагической анемии. Признаки, симптомы и тяжесть
(включая летальный исход) варьируют в зависимости от локализации и
степени тяжести или массивности кровотечения и/или анемии.
Кровотечения из слизистых оболочек
(например, носовое, десневое, желудочно-кишечное, из мочеполового
тракта включая патологическое вагинальное и усиленное менструальное
кровотечение) и анемия часто отмечались при длительном лечении
Ксарелто® в
сравнении с лечением антагонистами витамина K (АВК). Следовательно, в
дополнение к адекватному клиническому осмотру, при необходимости, для
выявления скрытого кровотечения может иметь значение лабораторное
определение уровня гемоглобина/гематокрита и количественная оценка
клинической значимости явного кровотечения.
Риск
развития кровотечения может быть повышен у некоторых групп пациентов,
например, с неконтролируемой тяжелой артериальной гипертензией и/или
получающих сопутствующее лечение препаратами, влияющими на гемостаз.
Менструальные кровотечения могут быть более длительными и
интенсивными. Геморрагические осложнения могут проявляться слабостью,
бледностью, головокружением, головной болью, необъяснимой
припухлостью, одышкой или необъяснимым шоковым состоянием. В
некоторых случаях, вследствие анемии наблюдались симптомы ишемии
миокарда, такие как боли за грудиной или стенокардия.
При
применении Ксарелто®
вследствие тяжелого кровотечения регистрировались и такие известные
осложнения как компартмент-синдром и почечная недостаточность в
результате гипоперфузии. Поэтому при оценке состояния любого
пациента, получающего антикоагулянты, следует рассматривать
возможность кровоизлияния.
При
возникновении нежелательных лекарственных реакций обращаться к
медицинскому работнику, фармацевтическому работнику или напрямую в
информационную базу данных по нежелательным реакциям (действиям) на
лекарственные препараты, включая сообщения о неэффективности
лекарственных препаратов
РГП
на ПХВ «Национальный Центр экспертизы лекарственных средств и
медицинских изделий» Комитет контроля качества и безопасности
товаров и услуг Министерства здравоохранения Республики Казахстан
http://www.ndda.kz
Дополнительные
сведения
Состав лекарственного препарата
Одна
таблетка содержит
активное
вещество —
ривароксабана
микронизированного
10 мг,
вспомогательные
вещества: целлюлоза
микрокристаллическая, натрия кроскармеллоза, гипромеллоза 5сР
(гидроксипропилметилцеллюлоза
2910),
лактозы моногидрат, магния стеарат, натрия лаурилсульфат,
состав
оболочки: железа
(ІІІ)
оксид
красный
(Е172),
гипромеллоза 15 сР
(гидроксипропилметилцеллюлоза
2910),
макрогол 3350 (полиэтиленгликоль
(3350)),
титана диоксид
(Е171).
Описание
внешнего вида, запаха, вкуса
Таблетки круглой формы, с двояковыпуклой
поверхностью, покрытые пленочной оболочкой светло-красного цвета, с
треугольником и маркировкой «10» на одной стороне и
фирменным крестом «BAYER» на другой стороне.
Форма выпуска и упаковка
По
5 и по 10 таблеток в контурную ячейковую упаковку из Ал/ПП или
Ал/ПВХ. По 1 контурной ячейковой упаковке с 5 таблетками, 1, 3 или 10
контурных ячейковых упаковок с 10 таблетками вместе
с инструкцией по медицинскому применению на государственном и русском
языках помещают в картонную пачку.
Срок хранения
3
года
Не
применять по истечении срока годности.
Условия хранения
Хранить
при температуре не выше 30о
С.
Хранить
в недоступном для детей месте!
Условия отпуска из аптек
По
рецепту
Сведения
о производителе
Байер АГ, Кайзер-Вильгельм Аллее
51368 Леверкузен, Германия
тел.:
0214/30 51 348
факс:
0214/30 51 603
e-mail:
medical-information@bayer.com
Держатель
регистрационного удостоверения
Байер АГ, Кайзер-Вильгельм Аллее
51368 Леверкузен, Германия
тел.:
0214/30 51 348
факс:
0214/30 51 603
e-mail:
medical-information@bayer.com
Наименование,
адрес и контактные данные (телефон, факс, электронная почта)
организации на территории Республики Казахстан, принимающей претензии
(предложения) по качеству лекарственных средств от потребителей
ТОО «Байер КАЗ»
ул. Тимирязева, 42, павильон 15,
050057 Алматы, Республика Казахстан,
тел. +7 727 258
80 40, факс: +7 727 258
80 39,
e-mail:
kz.claims@bayer.com
Наименование,
адрес и контактные данные (телефон, факс, электронная почта)
организации на территории Республики Казахстан ответственной за
пострегистрационное наблюдение за безопасностью лекарственного
средства
ТОО
«Байер КАЗ»
ул.
Тимирязева 42, павильон 15,
050057,
Алматы, Республика Казахстан
тел:
+7 701 715 78 46 (круглосуточно)
тел:
+7 727 258 80 40, вн. 106 (в рабочие часы)
факс:
+7 727 2588 039
e-mail: pv.centralasia@bayer.com
| Ксарелто_10мг_рус.docx | 0.06 кб |
| Ксарелто_10мг_каз.docx | 0.1 кб |
Отправить прикрепленные файлы на почту
Способ применения и дозы
Внутрь, независимо от приема пищи.
Если пациент не способен проглотить таблетку целиком, таблетку Ксарелто® можно измельчить и смешать с водой или жидким питанием, например, яблочным пюре, непосредственно перед приемом внутрь.
Измельченную таблетку Ксарелто® можно ввести через желудочный зонд. Положение зонда в ЖКТ необходимо дополнительно согласовать с врачом перед приемом Ксарелто®. Измельченную таблетку следует вводить через желудочный зонд в небольшом количестве воды, после чего необходимо ввести небольшое количество воды для того, чтобы смыть остатки препарата со стенок зонда.
Профилактика ВТЭ у пациентов, подвергающихся большим ортопедическихм операциям на нижних конечностях
Рекомендуется назначать по 10 мг (1 таб.) 1 раз/сут. Начальную дозу следует принять через 6-10 ч после операции при условии достигнутого гемостаза.
Продолжительность лечения:
- 5 недель — после большой операции на тазобедренном суставе;
- 2 недели — после большой операции на коленном суставе.
Действия при пропуске приема препарата
В случае пропуска приема препарата пациенту следует принять таблетку препарата Ксарелто® дозировкой 10 мг немедленно и на следующий день продолжить лечение по 1 таб./сут, как и ранее.
Профилактика рецидивов ТГВ или ТЭЛА после как минимум 6 месяцев лечения ТГВ или ТЭЛА
После как минимум 6 месяцев лечения тромбоза глубоких вен или тромбоэмболии легочной артерии рекомендуемая доза препарата Ксарелто® составляет 10 мг 1 раз/сут или 20 мг** 1 раз/сут, в зависимости от индивидуального соотношения риска рецидива ТГВ или ТЭЛА и риска кровотечения.
Таблица 1.
| Период | Схема приема | Суммарная суточная доза |
| Лечение и профилактика рецидивов ТГВ или ТЭЛА | ||
| от 1 до 21 дня | 15* мг 2 раза/сут | 30 мг |
| После 22 дня | 20** мг 1 раз/сут | 20 мг |
| Профилактика рецидивов ТГВ или ТЭЛА | ||
|
После как минимум 6 месяцев лечения ТГВ или ТЭЛА |
10 мг 1 раз/сут или 20** мг 1 раз/сут |
10 мг или 20 мг |
* В случае необходимости приема препарата в дозе 15 мг следует применять препарат Ксарелто®, выпускаемый в соответствующей дозировке, т.к. таблетки препарата с дозировкой 10 мг выпускаются без риски.
** В случае необходимости приема препарата в дозе 20 мг следует применять препарат Ксарелто®, выпускаемый в соответствующей дозировке.
Препарат Ксарелто® в дозировках 15 мг и 20 мг следует принимать во время еды, в дозировке 10 мг — независимо от приема пищи.
Действия при пропуске приема препарата
Необходимо следовать назначенной схеме приема препарата.
В случае пропуска приема препарата при назначении препарата Ксарелто® в дозе 15 мг 2 раза/сут, следует немедленно принять пропущенную таблетку, чтобы обеспечить прием суммарной суточной дозы препарата, составляющей 30 мг. В этом случае допускается принять 2 таб. по 15 мг в один прием. На следующий день необходимо продолжить лечение в соответствии с рекомендованной схемой приема препарата.
В случае пропуска приема препарата при назначении препарата Ксарелто® 1 раз/сут следует немедленно принять пропущенную таблетку, чтобы обеспечить прием суточной дозы препарата. На следующий день необходимо продолжить лечение в соответствии с рекомендованной схемой приема препарата.
Отдельные группы пациентов
Коррекция дозы в зависимости от возраста больного (старше 65 лет), пола, массы тела или этнической принадлежности не требуется.
Безопасность и эффективность применения у детей и подростков в возрасте до 18 лет не установлены.
- Пациенты с нарушением функции печени
Ривароксабан противопоказан пациентам с заболеваниями печени, сопровождающимися коагулопатией, которая обусловливает клинически значимый риск кровотечения.
Пациентам с другими заболеваниями печени изменения дозы не требуются.
Имеющиеся ограниченные клинические данные, полученные у пациентов со среднетяжелой печеночной недостаточностью (класс В по Чайлд-Пью), указывают на значимое усиление фармакологической активности препарата. У пациентов с тяжелой печеночной недостаточностью (класс С по Чайлд-Пью) клинические данные отсутствуют.
- Пациенты с нарушением функции почек
Имеющиеся ограниченные клинические данные демонстрируют значительное повышение концентрации ривароксабана у пациентов с тяжелой степенью нарушения функции почек (КК 15-29 мл/мин). Для лечения этой категории пациентов препарат Ксарелто® следует применять с осторожностью.
Применение ривароксабана не рекомендуется у пациентов с КК менее 15 мл/мин.
- При назначении препарата Ксарелто® с целью профилактики ВТЭ пациентам, подвергающимся большим ортопедическим оперативным вмешательствам на нижних конечностях, с легкой или средней степенью нарушения функции почек (КК 50-80 мл/мин или 30-49 мл/мин, соответственно), коррекция дозы не требуется.
- При назначении препарата Ксарелто® с целью лечения и профилактики рецидивов ТГВ или ТЭЛА пациентам с легкой степенью нарушения функции почек (КК 50-80 мл/мин) коррекция дозы не требуется. Пациентам со средней (КК 30-49 мл/мин) или тяжелой (КК 15-29 мл/мин) степенью нарушения функции почек следует принимать препарат Ксарелто® в дозе 15 мг 2 раза/сут на протяжении первых 3 недель. Впоследствии, когда рекомендуемая доза препарата Ксарелто® составит 20 мг 1 раз/сут, следует предусмотреть снижение дозы до 15 мг 1 раз/сут, если риск возникновения кровотечения выше риска рецидивов ТГВ и ТЭЛА. Рекомендации но применению препарата Ксарелто® в дозе 15 мг основаны на фармакокинетическом моделировании и в клинических исследованиях не изучались. При применении препарата Ксарелто® в дозировке 10 мг коррекция дозы не требуется.
Примечание: Информация о применении препарата Ксарелто® в дозе 10 мг 1 раз/сут пациентам с фибрилляцией предсердий неклапанного происхождения, перенесших чрескожное коронарное вмешательство (ЧКВ) с установкой стента и имеющих среднюю степень нарушения функции почек (КК 30-49 мл/мин), размещена в инструкции по медицинскому применению лекарственного препарата Ксарелто® 15/20 мг (per. номер ЛП-001457).
Перевод пациентов с лечения антагонистами витамина К (АВК) на препарат Ксарелто®
При переводе пациентов с АВК на Ксарелто®, значения MHO будут ложно повышенными после приема препарата Ксарелто®. Поэтому показатель MHO не следует использовать для контроля антикоагулянтного эффекта Ксарелто® (см. раздел «Лекарственное взаимодействие»).
При профилактике инсульта и системной тромбоэмболии следует прекратить лечение АВК и начать лечение препаратом Ксарелто® при величине МНО ≤ 3.
При ТГВ и ТЭЛА следует прекратить лечение АВК и начать лечение препаратом Ксарелто® при величине МНО ≤ 2.5.
Перевод пациентов с препарата Ксарелто® на лечение АВК
Существует вероятность недостаточного антикоагулянтного эффекта при переходе с Ксарелто® на АВК. В переходный период, связанный с переводом на другой противосвертывающий препарат, необходимо обеспечить непрерывный и достаточный антикоагулянтный эффект. Следует иметь в виду, что Ксарелто® может способствовать повышению показателя МНО.
При переводе пациента с Ксарелто® на АВК, оба препарата следует давать одновременно до тех пор, пока MHO не достигнет ≥2. В течение первых двух дней переходного периода следует применять стандартную дозу АВК, а впоследствии руководствоваться значением МНО. В период совместного приема Ксарелто® и АВК MHO следует определять не ранее чем через 24 ч после предыдущего приема, но до приема следующей дозы Ксарелто®. После отмены препарата Ксарелто® определение MHO с достаточной степенью надежности возможно через 24 ч после приема последней дозы препарата (см. раздел «Лекарственное взаимодействие»).
Перевод пациентов с парентеральных антикоагулянтов на препарат Ксарелто®
При переводе пациента с парентеральных антикоагулянтов на препарат Ксарелто® прием препарата Ксарелто® следует начинать за 0-2 ч до предполагаемого введения следующей дозы парентерального препарата (например, низкомолекулярного гепарина) или во время отмены длительно применяемого парентерального препарата (например, в/в нефракционированного гепарина).
Перевод пациентов с препарата Ксарелто® на парентеральные антикоагулянты
Следует отменить Ксарелто® и ввести первую дозу парентерального антикоагулянта во время предполагаемого приема следующей дозы препарата Ксарелто®.
Условия хранения
Препарат следует хранить в недоступном для детей месте при температуре не выше 30°С.
Срок годности
3 года. Не использовать по истечении срока годности.
Особые указания
Применение сопутствующих препаратов
Применение ривароксабана не рекомендуется у пациентов, получающих сопутствующее системное лечение противогрибковыми препаратами группы азолов (например, кетоконазолом) или ингибиторами ВИЧ-протеазы (например, ритонавиром). Эти препараты являются сильными ингибиторами CYP3A4 и Р-гликопротеина. Таким образом, данные препараты могут повышать концентрацию ривароксабана в плазме крови до клинически значимых значений (в 2.6 раза в среднем), что может привести к повышенному риску кровотечений.
Однако противогрибковый препарат группы азолов флуконазол, умеренный ингибитор CYP3A4, оказывает менее выраженное действие на экспозицию ривароксабана и может применяться с ним одновременно.
Нарушение функции почек
Ривароксабан следует с осторожностью применять у пациентов со средней степенью нарушения функции почек (КК 30-49 мл/мин), получающих сопутствующие препараты, которые могут приводить к повышению концентрации ривароксабана в плазме. У пациентов с тяжелой степенью нарушения функции почек (КК<30 мл/мин) концентрация ривароксабана в плазме может быть значительно повышена (в 1.6 раза в среднем), что может привести к повышенному риску кровотечения. Вследствие основного заболевания у таких пациентов имеется повышенный риск развития как кровотечения, так и тромбоза. В связи с ограниченным количеством клинических данных, препарат Ксарелто® следует применять с осторожностью у пациентов с КК 15-29 мл/мин. Клинические данные о применении ривароксабана у пациентов с тяжелым нарушением функции почек (КК <15 мл/мин) отсутствуют. Поэтому применение препарата Ксарелто® у таких пациентов не рекомендуется.
За пациентами с тяжелым нарушением функции почек (КК 15-29 мл/мин) или повышенным риском кровотечения, а также пациентами, получающими сопутствующее системное лечение противогрибковыми препаратами группы азолов или ингибиторами ВИЧ-протеаз, необходимо проводить тщательное наблюдение на предмет наличия признаков кровотечения после начала лечения.
Наблюдение может осуществляться путем проведения регулярного физикального обследования пациентов, тщательного контроля за состоянием дренажа послеоперационной раны, а также путем периодического определения гемоглобина.
Оперативные вмешательства при переломе проксимальных отделов бедренной кости
Применение Ксарелто® при оперативных вмешательствах по поводу перелома проксимальных отделов бедренной кости не изучалось в интервенционных клинических исследованиях. Имеются ограниченные клинические данные, полученные в наблюдательных исследованиях, у пациентов, подвергающихся оперативным вмешательствам при переломе нижних конечностей, в т.ч. при переломе проксимальных отделов бедренной кости.
Риск кровотечения
Как и при приеме других антикоагулянтов необходимо тщательно наблюдать пациентов, принимающих препарат Ксарелто®, для выявления признаков кровотечения.
В случае тяжелого кровотечения прием препарата Ксарелто® следует прекратить.
В клинических исследованиях кровотечения из слизистых оболочек (а именно: кровотечение из носа, десен, ЖКТ, мочеполовой системы, включая аномальное вагинальное или усиленное менструальное кровотечение) и анемия наблюдались чаще при длительном лечении ривароксабаном по сравнению с лечением АВК. Таким образом, в дополнение к надлежащему клиническому наблюдению, лабораторное исследование гемоглобина/гематокрита может быть значимым для выявления скрытых кровотечений и количественной оценки клинической значимости явных кровотечений, которые будут сочтены допустимыми.
Ксарелто®, как и другие антитромботические средства, следует с осторожностью применять у пациентов, имеющих повышенный риск кровотечений, в т.ч.:
- пациентов с врожденной или приобретенной склонностью к кровотечениям;
- пациентов с неконтролируемой тяжелой артериальной гипертензией;
- пациентов с язвенной болезнью желудка и двенадцатиперстной кишки в фазе обострения;
- пациентов, недавно перенесших язвенную болезнь желудка и двенадцатиперстной кишки;
- пациентов с сосудистой ретинопатией;
- пациентов, недавно перенесших внутричерепное или внутримозговое кровоизлияние;
- пациентов с патологией сосудов головного или спинного мозга;
- пациентов, недавно перенесших операцию на головном, спинном мозге или глазах;
- пациентов с бронхоэктазами или легочным кровотечением в анамнезе.
Следует соблюдать осторожность, если пациент одновременно получает лекарственные препараты, влияющие на гемостаз, такие как НПВП, ингибиторы агрегации тромбоцитов, другие антитромботические препараты или СИОЗС и СИОЗСН.
Пациентам с риском развития язвенной болезни желудка и двенадцатиперстной кишки может быть назначено соответствующее профилактическое лечение.
При необъяснимом снижении гемоглобина или АД необходимо искать источник кровотечения.
Терапия ривароксабаном не требует рутинного мониторинга его экспозиции. Тем не менее измерение концентрации ривароксабана с помощью калиброванного теста для количественного определения анти-Ха активности, может оказаться полезным в исключительных случаях, когда информация об экспозиции ривароксабана может быть использована при принятии клинически значимых решений, например, в случае передозировки или экстренного хирургического вмешательства.
Удлинение корригированного интервала QT
На фоне лечения ривароксабаном удлинение интервала QT не наблюдалось.
Спинальная анестезия
При выполнении эпидуральной/спинальной анестезии или спинномозговой пункции у пациентов, получающих ингибиторы агрегации тромбоцитов с целью профилактики тромбоэмболических осложнений, существует риск развития эпидуральной или спинномозговой гематомы, которая может привести к длительному параличу. Риск этих событий в дальнейшем повышается при применении постоянного эпидурального катетера или сопутствующей терапии лекарственными препаратами, влияющими на гемостаз. Травматичное выполнение эпидуральной или спинномозговой пункции или повторная пункция также могут способствовать повышению риска.
Пациенты должны находиться под наблюдением для выявления признаков и симптомов неврологических нарушений (например, онемение или слабость ног, дисфункция кишечника или мочевого пузыря). При обнаружении неврологических расстройств необходима срочная диагностика и лечение.
Врач должен сопоставить потенциальную пользу и риск перед проведением спинномозгового вмешательства пациентам, получающим антикоагулянты или которым планируется назначение антикоагулянтов с целью профилактики тромбозов.
С целью снижения потенциального риска кровотечения, ассоциированного с одновременным применение ривароксабана и эпидуральной/спинальной анестезии или спинальной пункции, следует учитывать фармакокинетический профиль ривароксабана. Установку или удаление эпидурального катетера или люмбальную пункцию лучше проводить тогда, когда антикоагулянтный эффект ривароксабана оценивается как слабый.
Эпидуральный катетер извлекают не ранее чем через 18 ч после назначения последней дозы ривароксабана. Ксарелто® не следует назначать ранее чем через 6 ч после извлечения эпидурального катетера. В случае травматичной пункции назначение препарата Ксарелто® следует отложить на 24 ч.
Хирургические операции и вмешательства
Если необходимо проведение инвазивной процедуры или хирургического вмешательства, прием Ксарелто® следует прекратить, по крайней мере, за 24 ч до вмешательства, если это возможно, и на основании заключения врача. Если процедуру нельзя отложить, повышенный риск кровотечения следует оценивать в сравнении с необходимостью срочного вмешательства.
Прием препарата Ксарелто® следует возобновить после инвазивной процедуры или хирургического вмешательства при условии наличия соответствующих клинических показателей и адекватного гемостаза.
Женщины репродуктивного возраста
Препарат Ксарелто® можно принимать женщинам детородного возраста только при условии применения эффективных методов контрацепции.
Кожные реакции
При проведении постмаркетинговых наблюдений сообщалось о случаях возникновения синдрома Стивенса-Джонсона и токсического эпидермального некролиза. При первом появлении тяжелой кожной сыпи (например, при ее распространении, интенсификации и/или образовании волдырей) или при наличии других симптомов гиперчувствительности, связанных с поражением слизистой оболочки, следует прекратить терапию препаратом Ксарелто®.
Пациенты с искусственными клапанами сердца
Основываясь на данных рандомизированного контролируемого клинического исследования по сравнению терапии препаратом Ксарелто® и антитромбоцитарной терапии, применение препарата Ксарелто® не рекомендуется для профилактики тромбозов у пациентов, перенесших недавнюю транскатетерную замену аортального клапана (TAVR). Безопасность и эффективность применения препарата Ксарелто® не изучались у пациентов с какими-либо другими искусственными клапанами сердца или у пациентов после иных вмешательств на клапанах сердца, следовательно, нет данных, подтверждающих, что применение препарата Ксарелто® обеспечивает достаточный антикоагулянтный эффект у данных категорий пациентов.
Пациенты с высоким риском тройного позитивного антифосфолипидного синдрома
Применение препарата Ксарелто® не рекомендуется у пациентов, имеющих тромбозы в анамнезе, у которых диагностирован устойчивый тройной позитивный антифосфолипидный синдром (наличие волчаночного антикоагулянта, антител к кардиолипину и антител к бета-2-гликопротеину I), поскольку терапия ривароксабаном сопровождается повышенной частотой рецидивов тромботических событий в сравнении с терапией АВК.
Пациенты с гемодинамически нестабильной ТЭЛА и пациенты, которым требуется проведение тромболизиса или тромбэктомии
Ривароксабан не рекомендуется в качестве альтернативы нефракционированному гепарину у пациентов с гемодинамически нестабильной тромбоэмболией легочной артерии, а также у пациентов, которые могут нуждаться в проведении тромболизиса или тромбэктомии, поскольку безопасность и эффективность препарата Ксарелто® при таких клинических ситуациях не установлена.
Данные по безопасности, полученные из доклинических исследований
За исключением эффектов, связанных с усилением фармакологического действия (кровотечений), при анализе доклинических данных, полученных в исследованиях по фармакологической безопасности, специфической опасности для человека не обнаружено.
Описание
Антикоагулянт — прямой ингибитор фактора Xa.
Лекарственная форма
Таблетки, покрытые пленочной оболочкой розового цвета, круглые, двояковыпуклые; методом выдавливания нанесена гравировка: на одной стороне — треугольник с обозначением дозировки «10», на другой — фирменный байеровский крест.
Применение у детей
Противопоказано применение в детском и подростковом возрасте до 18 лет.
Фармакодинамика
Механизм действия
Ривароксабан — высокоселективный прямой ингибитор фактора Ха, обладающий высокой биодоступностью при приеме внутрь.
Активация фактора X с образованием фактора Ха через внутренний и внешний пути свертывания играет центральную роль в коагуляционном каскаде. Фактор Ха является компонентом формирующегося протромбиназного комплекса, действие которого приводит к превращению протромбина в тромбин. В результате эти реакции приводят к формированию фибринового тромба и активации тромбоцитов тромбином. Одна молекула фактора Ха катализирует образование более 1000 молекул тромбина, что получило название «тромбинового взрыва». Скорость реакции связанного в протромбиназе фактора Ха увеличивается в 300000 раз по сравнению с таковой свободного фактора Ха, что обеспечивает резкий скачок в уровне тромбина. Селективные ингибиторы фактора Ха могут остановить «тромбиновый взрыв». Таким образом, ривароксабан оказывает влияние на результаты некоторых специфических или общих лабораторных исследований, применяемых для оценки свертывающих систем.
Фармакодинамические эффекты
У человека наблюдалось дозозависимое ингибирование фактора Ха. Ривароксабан оказывает дозозависимое влияние на протромбиновое время и близко коррелирует с концентрациями в плазме (r=0.98), если для анализа используется набор Neoplastin. При использовании других реактивов результаты будут отличаться. Протромбиновое время следует измерять в секундах, поскольку MHO откалибровано и сертифицировано только для производных кумарина и не может применяться для других антикоагулянтов.
У пациентов, которым проводятся большие ортопедические операции, 5/95-процентили для протромбинового времени (Neoplastin) через 2-4 ч после приема таблетки (т.е. на максимуме эффекта) варьируют от 13 до 25 сек.
У пациентов, получающих ривароксабан для лечения и профилактики рецидивов тромбоза глубоких вен (ТГВ) и тромбоэмболии легочной артерии (ТЭЛА), 5/95-процентили для протромбинового времени (Neoplastin) через 2-4 ч после приема таблетки (т.е. на максимуме эффекта) варьируют от 17 до 32 сек у пациентов, принимающих 15 мг 2 раза/сут, и от 15 до 30 сек у пациентов, принимающих 20 мг 1 раз/сут.
Также ривароксабан дозозависимо увеличивает АЧТВ и результат HepTest; однако эти параметры не рекомендуется использовать для оценки фармакодинамических эффектов ривароксабана.
В период лечения ривароксабаном проводить мониторинг параметров свертывания крови не требуется. Однако если для этого есть клиническое обоснование (например, при передозировке препарата или в случае необходимости экстренного хирургического вмешательства), концентрация ривароксабана может быть измерена при помощи калиброванного количественного теста анти-фактора Ха (например, STA-Liquid Anti-Xa, производитель Диагностика Стаго САС, Франция или аналогичный).
У здоровых мужчин и женщин старше 50 лет удлинение интервала QT под влиянием ривароксабана не наблюдалось.
Побочные действия
Безопасность препарата оценивалась в тринадцати исследованиях III фазы, включавших 53103 пациента, принимавших препарат Ксарелто®.
Таблица 2. Число пациентов, участвовавших в исследовании и принявших как минимум 1 дозу ривароксабана, суммарная суточная доза и максимальная продолжительность лечения в клинических исследованиях 111 фазы с использованием препарата Ксарелто®
| Число пациентов* | Суммарная суточная доза | Максимальная продолжительность лечения |
| Профилактика венозной тромбоэмболии (ВТЭ) у пациентов, перенесших плановую операцию по замене тазобедренного или коленного сустава | ||
| 6097 | 10 мг | 39 дней |
| Профилактика венозной тромбоэмболии у госпитализированных по медицинским показаниям пациентов | ||
| 3997 | 10 мг | 39 дней |
| Лечение ТГВ, ТЭЛА и профилактика рецидивов ТГВ, ТЭЛА | ||
| 6790 |
День 1-21: 30 мг Начиная с 22 дня: 20 мг После минимум 6 месяцев терапии: 10 мг или 20 мг |
21 месяц |
| Профилактика инсульта и системной эмболии у пациентов с фибрилляцией предсердий неклапанного происхождения | ||
| 7750 | 20 мг | 41 месяц |
| Профилактика атеротромботических осложнений у пациентов после острого коронарного синдрома (ОКС) | ||
| 10225 | 5 мг или 10 мг соответственно, в комбинации с ацетилсалициловой кислотой или ацетилсалициловой кислотой с клопидогрелом или тиклопидином | 31 месяц |
| Профилактика инсульта, инфаркта миокарда и смерти вследствие сердечно-сосудистых причин, а также для профилактики острой ишемии конечностей и общей смертности у пациентов с ИБС или ЗПА | ||
| 18244 | 5 мг в комбинации с ацетилсалициловой кислотой 100 мг или 10 мг в монотерапии | 47 месяцев |
* Пациенты, получившие по меньшей мере одну дозу ривароксабана.
Таблица 3. Частота возникновения кровотечений и анемии у пациентов, получавших лечение препаратом Ксарелто® в клинических исследованиях III фазы
| Количество пациентов | |
| Любое кровотечение | Анемия |
| Профилактика венозной тромбоэмболии (ВТЭ) у пациентов, перенесших плановую операцию по замене тазобедренного или коленного сустава | |
| 6.8% | 5.9% |
| Профилактика венозной тромбоэмболии у госпитализированных по медицинским показаниям пациентов | |
| 12.6% | 2.1% |
| Лечение ТГВ, ТЭЛА и профилактика рецидивов ТГВ, ТЭЛА | |
| 23% | 1.6% |
| Профилактика инсульта и системной тромбоэмболии у пациентов с фибрилляцией предсердий неклапанного происхождения | |
| 28 событий на 100 пациенто-лет | 2.5 события на 100 пациенто-лет |
| Профилактика атеротромбических осложнений у пациентов после острого коронарного синдрома (ОКС) | |
| 22 события на 100 пациенто-лет | 1.4 события на 100 пациенто-лет |
| Профилактика инсульта, инфаркта миокарда и смерти вследствие сердечно-сосудистых причин, а также для профилактики острой ишемии конечностей и общей смертности у пациентов с ИБС или ЗПА | |
| 6.7 события на 100 пациенто-лет | 0.15 события на 100 пациенто-лет* |
* При сборе данных о нежелательных явлениях применялся предустановленный выборочный подход.
Учитывая механизм действия, применение препарата Ксарелто® может сопровождаться повышенным риском скрытого или явного кровотечения из любых органов и тканей, которое может приводить к постгеморрагической анемии. Риск развития кровотечений может увеличиваться у пациентов с неконтролируемой артериальной гипертензией и/или при совместном применении с препаратами, влияющими на гемостаз (см. раздел «С осторожностью»). Признаки, симптомы и степень тяжести (включая возможный летальный исход) варьируют в зависимости от локализации, степени тяжести или продолжительности кровотечения и/или анемии (см. раздел «Передозировка»).
Геморрагические осложнения могут проявляться в виде слабости, бледности, головокружения, головной боли или необъяснимых отеков, одышки или шока, развитие которого нельзя объяснить другими причинами. В некоторых случаях вследствие анемии развивались симптомы ишемии миокарда, такие как боль в груди и стенокардия.
При применении препарата Ксарелто® регистрировались и такие известные осложнения, вторичные по отношению к тяжелым кровотечениям, как синдром повышенного субфасциального давления (компартмент-синдром) и почечная недостаточность вследствие гипоперфузии. Таким образом, следует учитывать возможность кровотечения при оценке состояния любого пациента, получающего антикоагулянты.
Частота встречаемости НЛР (нежелательных лекарственных реакций) при применении препарата Ксарелто® приведена в таблице ниже. В рамках каждой группы, выделенной по частоте, нежелательные явления представлены в порядке уменьшения их серьезности.
Частота встречаемости определяется как: очень часто (≥1/10), часто (от ≥1/100 до <1/10), нечасто (от ≥1/1000 до <1/100), редко (от ≥1/10000 до <1/1000).
Таблица 4. Все возникшие на фоне лечения нежелательные лекарственные реакции, зарегистрированные у пациентов в клинических исследованиях III фазы (кумулятивные данные RECORD 1-4, ROCKET AF, J-ROCKET, MAGELLAN, ATLAS, EINSTEIN (DVT/PE/Extension/CHOICE) и COMPASS*)
| Часто | Нечасто | Редко |
| Со стороны крови и лимфатической системы | ||
| Анемия (включая соответствующие лабораторные показатели) | Тромбоцитоз (включая повышенное содержание тромбоцитов)A | |
| Со стороны иммунной системы | ||
| Аллергическая реакция, аллергический дерматит | ||
| Cо стороны нервной системы | ||
| Головокружение, головная боль | Внутримозговое и внутричерепное кровоизлияние, обморок | |
| Со стороны органа зрения | ||
| Кровоизлияние в глаз (включая кровоизлияние в конъюнктиву) | ||
| Со стороны сердца | ||
| Тахикардия | ||
| Со стороны сосудов | ||
| Снижение АД, гематома | ||
| Со стороны дыхательной системы | ||
| Носовое кровотечение, кровохарканье | ||
| Со стороны пищеварительной системы | ||
| Кровоточивость десен, желудочно-кишечное кровотечение (включая ректальное кровотечение), боль в животе, диспепсия, тошнота, запорА, диарея, рвотаА | Сухость во рту | |
| Со стороны печени и желчевыводящих путей | ||
| Нарушение функции печени | Желтуха | |
| Со стороны кожи и подкожных тканей | ||
| Кожный зуд (включая нечастые случаи генерализованного зуда), кожная сыпь, экхимоз, кожные и подкожные кровоизлияния | Крапивница | |
| Со стороны костно-мышечной системы и соединительной ткани | ||
| Боль в конечностяхА | Гемартроз | Кровоизлияние в мышцу |
| Со стороны почек и мочевыводящих путей | ||
| Кровотечение из урогенитального тракта (включая гематурию), нарушение функции почек (включая повышение концентрации креатинина, повышение концентрации мочевины крови)А | ||
| Со стороны половой системы | ||
| Кровотечение из урогенитального тракта (включая меноррагиюв) | ||
| Общие расстройства | ||
| ЛихорадкаА, периферический отек, снижение общей мышечной силы и тонуса (включая слабость и астению) | Ухудшение общего самочувствия (включая недомогание) | Локальный отекА |
| Лабораторные и инструментальные данные | ||
| Повышение активности печеночных трансаминаз | Повышение концентрации билирубина, повышение активности ЩФА, повышение активности ЛДГА, повышение активности липазыА, повышение активности амилазыА, повышение активности ГГТА | Повышение концентрации конъюгированного билирубина (с соответствующим повышением активности АЛТ или без него) |
| Травмы, интоксикации и осложнения манипуляций | ||
| Кровотечение после медицинской манипуляции (включая послеоперационную анемию и кровотечение из раны), гематома | Выделение секрета из раныА | Сосудистая псевдоаневризмаС |
А Наблюдались после больших ортопедических операций на нижних конечностях.
В Регистрировались при лечении ВТЭ как очень частые у женщин моложе 55 лет.
С Регистрировались как нечастые в рамках профилактики осложнений при ОКС (после проведения чрескожных вмешательств).
* Применялся предварительно заданный избирательный подход к сбору данных по нежелательным явлениям. Т.к. частота нежелательных лекарственных реакций не повысилась, и т.к. никаких новых нежелательных лекарственных реакций идентифицировано не было, данные из исследования COMPASS не были включены для расчета частоты в данной таблице.
Во время пострегистрационного мониторинга сообщалось о случаях приведенных ниже нежелательных реакций, развитие которых имело временную связь с приемом препарата Ксарелто®. Оценить частоту встречаемости таких нежелательных реакций в рамках пострегистрационного мониторинга не представляется возможным.
Со стороны иммунной системы: ангионевротический отек, аллергический отек. В рамках регистрационных клинических исследований (РКИ) III фазы такие нежелательные реакции были расценены как нечастые (от ≥1/1000 до <1/100).
Со стороны печени и желчевыводящих путей: холестаз, гепатит (включая гепатоцеллюлярное повреждение). В рамках РКИ III фазы такие нежелательные реакции были расценены как редкие (от ≥1/10000 до <1/1000).
Со стороны кровеносной и лимфатической системы: тромбоцитопения. В рамках РКИ III фазы такие нежелательные реакции были расценены как нечастые (от ≥1/1000 до <1/100).
Применение при беременности и кормлении грудью
Беременность
Эффективность и безопасность применения ривароксабана у беременных не установлены. Данные, полученные в экспериментальных исследованиях на животных, показали выраженную токсичность ривароксабана для материнского организма, связанную с фармакологическим действием препарата (например, осложнения в форме кровоизлияний) и приводящую к репродуктивной токсичности. Первичного тератогенного потенциала не обнаружено.
Вследствие возможного риска развития кровотечения и способности проникать через плацентарный барьер ривароксабан противопоказан при беременности.
Женщинам с сохраненной репродуктивной способностью следует использовать эффективные методы контрацепции в период лечения ривароксабаном.
Период грудного вскармливания
Эффективность и безопасность применения Ксарелто® у женщин в период лактации не установлены. Данные, полученные в экспериментальных исследованиях на животных, показывают, что ривароксабан выделяется с грудным молоком. Ривароксабан может применяться только после отмены грудного вскармливания.
Фертильность
Исследования показали, что ривароксабан не влияет на мужскую и женскую фертильность у крыс. Исследований влияния ривароксабана на фертильность у человека не проводилось.
Взаимодействие
Фармакокинетическое взаимодействие
Выведение ривароксабана осуществляется главным образом посредством метаболизма в печени, опосредованного системой цитохрома Р450 (CYP3A4, CYP2J2), а также — путем почечной экскреции неизмененного лекарственного вещества с использованием систем переносчиков P-gp/Bcrp (Р-гликопротеина/белка устойчивости к раку молочной железы).
Ингибирование CYP
Ривароксабан не ингибирует CYP3A4 или любые другие основные изоферменты CYP.
Индукция CYP
Ривароксабан не индуцирует CYP3A4 или любые другие основные изоферменты CYP.
Влияние на ривароксабан
Одновременное применение ривароксабана и мощных ингибиторов изофермента CYP3A4 и Р-гликопротеина может привести к снижению почечного и печеночного клиренса ривароксабана и, таким образом, значительно увеличить его системное воздействие.
Совместное применение ривароксабана и противогрибкового средства из группы азолов кетоконазола (400 мг 1 раз/сут), являющегося мощным ингибитором CYP3A4 и Р-гликопротеина, приводило к повышению средней равновесной AUC ривароксабана в 2.6 раза и увеличению средней Cmax ривароксабана в 1.7 раза, что сопровождалось значительным усилением фармакодинамического действия препарата.
Совместное назначение ривароксабана и ингибитора протеазы ВИЧ ритонавира (600 мг 2 раза/сут), являющегося мощным ингибитором CYP3A4 и Р-гликопротеина, приводило к увеличению средней равновесной AUC ривароксабана в 2.5 раза и увеличению средней Cmax ривароксабана в 1.6 раза, что сопровождалось значительным усилением фармакодинамического действия препарата. В связи с этим ривароксабан не рекомендуется к применению у пациентов, получающих системное лечение противогрибковыми препаратами группы азолов или ингибиторами протеазы ВИЧ.
Ожидается, что другие лекарственные вещества, сильно угнетающие только один из путей выведения ривароксабана – с участием CYP3A4 или Р-гликопротеина, будут увеличивать концентрацию ривароксабана в плазме до менее значимых значений.
Кларитромицин (500 мг 2 раза/сут), мощный ингибитор изофермента CYP3A4 и умеренный ингибитор Р-гликопротеина, вызывал увеличение значений AUC в 1.5 раза и Cmax ривароксабана в 1.4 раза. Это увеличение имеет порядок нормальной изменчивости AUC и Cmax и считается клинически незначимым.
Эритромицин (500 мг 3 раза/сут), умеренный ингибитор изофермента CYP3A4 и Р-гликопротеина, вызывал увеличение значений AUC и Cmax ривароксабана в 1.3 раза. Это увеличение имеет порядок нормальной изменчивости AUC и Cmax и считается клинически незначимым.
У пациентов с легкой степенью нарушения функции почек (КК 50-80 мл/мин) эритромицин (500 мг 3 раза/сут) вызывал увеличение значений AUC ривароксабана в 1.8 раза и Cmax в 1.6 раза по сравнению с пациентами с нормальной функцией почек, не получавших сопутствующей терапии. У пациентов со средней степенью нарушения функции почек (КК 30-49 мл/мин) эритромицин вызывал увеличение значений AUC ривароксабана в 2.0 раза и Cmax в 1.6 раза по сравнению с пациентами с нормальной функцией почек, не получавших сопутствующей терапии.
Флуконазол (400 мг 1 раз/сут), умеренный ингибитор изофермента CYP3A4, вызывал увеличение средней AUC ривароксабана в 1.4 раза и увеличение средней Cmax в 1.3 раза. Это увеличение имеет порядок нормальной изменчивости AUC и Cmax считается клинически незначимым.
Следует избегать одновременного применения ривароксабана с дронедароном в связи с ограниченностью клинических данных о совместном применении.
Совместное применение Ксарелто® и рифампицина, являющегося мощным индуктором CYP3A4 и Р-гликопротеина, приводило к снижению средней AUC ривароксабана приблизительно на 50% и параллельному уменьшению его фармакодинамических эффектов. Совместное применение ривароксабана с другими мощными индукторами CYP3A4 (например, фенитоином, карбамазепином, фенобарбиталом или препаратами зверобоя продырявленного) также может привести к снижению концентрации ривароксабана в плазме. Уменьшение концентрации ривароксабана в плазме признано клинически незначимым. Мощные индукторы CYP3A4 необходимо применять с осторожностью.
Фармакодинамическое взаимодействие
После одновременного применения эноксапарина натрия (однократная доза 40 мг) и препарата Ксарелто® (однократная доза 10 мг) наблюдался суммированный эффект в отношении активности анти-фактора Ха, не сопровождавшийся дополнительными суммированными эффектами в отношении проб на свертываемость крови (протромбиновое время, АЧТВ). Эноксапарин не изменял фармакокинетику ривароксабана.
После совместного применения препарата ривароксабана в дозе 15 мг и напроксена в дозе 500 мг клинически значимого увеличения времени кровотечения не наблюдалось. Тем не менее, у отдельных лиц возможен более выраженный фармакодинамический ответ.
Не обнаружено фармакокинетического взаимодействия между ривароксабаном в дозе 15 мг и клопидогрелом (нагрузочная доза 300 мг с последующим назначением поддерживающей дозы 75 мг), но у части пациентов обнаружено значимое увеличение времени кровотечения, не коррелировавшее со степенью агрегации тромбоцитов и содержанием Р-селектина или GPIIb/IIIa-рецептора.
Перевод пациентов с варфарина (МНО от 2 до 3) на ривароксабан (20 мг) или с ривароксабана (20 мг) на варфарин (МНО от 2 до 3 ) сопровождался более чем аддитивным увеличением протромбинового времени/МНО (Неопластин) (в отдельных случаях до 12), тогда как эффекты изменения аЧТВ, подавления активности фактора Xa и эндогенного потенциала тромбина (ЭПТ) были аддитивными.
Для оценки фармакодинамических эффектов препарата Ксарелто® в переходный период можно провести анализ анти-Ха факторной активности, PiCT и HepTest, если на определяемые в их ходе показатели не повлиял варфарин.
Начиная с 4-го дня после отмены варфарина, все анализы (включая ПВ, аЧТВ, подавление активности фактора Xa и ЭПТ) отражали исключительно эффект препарата Ксарелто®.
Для оценки фармакодинамических эффектов варфарина в переходный период можно использовать показатель МНО, измеренный в момент достижения Cmin ривароксабана (через 24 ч после приема дозы ривароксабана), т.к. в этот момент времени влияние ривароксабана на результаты анализа минимально.
Фармакокинетического взаимодействия между варфарином и препаратом Ксарелто® не обнаружено.
Лекарственное взаимодействие препарата Ксарелто® с антагонистом витамина К (АВК) фениндионом не изучалось. Рекомендуется по мере возможности избегать перевода пациентов с терапии препаратом Ксарелто® на терапию АВК фениндионом и наоборот.
Имеется ограниченный опыт перевода пациентов с терапии АВК аценокумаролом на препарат Ксарелто®.
Если возникает необходимость перевести пациента с терапии препаратом Ксарелто® на терапию АВК фениндионом или аценокумаролом, то следует соблюдать особую осторожность, в период совместного приема препарата Ксарелто® и АВК ежедневный контроль фармакодинамического действия препаратов (МНО, протромбиновое время) должен проводиться непосредственно перед приемом следующей дозы Ксарелто®.
Если возникает необходимость перевести пациента с терапии АВК фениндионом или аценокумаролом на терапию препаратом Ксарелто®, то следует соблюдать особую осторожность, контроль фармакодинамического действия препаратов при этом не требуется.
Как и в случае применения других антикоагулянтов, необходимо соблюдать осторожность при совместном применении препарата Ксарелто® с селективными ингибиторами обратного захвата серотонина (СИОЗС) и селективными ингибиторами обратного захвата серотонина и норэпинефрина (СИОЗСН), поскольку применение этих препаратов повышает риск кровотечения. Результаты клинических исследований продемонстрировали численное повышение больших и небольших клинически значимых кровотечений во всех группах лечения при совместном применении этих препаратов.
Сопутствующее применение других препаратов
Не отмечалось клинически значимых фармакокинетического или фармакодинамического взаимодействич при одновременном применении ривароксабана с мидазоламом (субстратом CYP3A4), дигоксином (субстратом Р-гликопротеина) или аторвастатином (субстратом CYP3A4 и P-gp).
Совместное применение с ингибитором протоновой помпы омепразолом, блокатором гистаминовых Н2-рецепторов ранитидином, антацидами алюминия гидроксидом/магния гидроксидом, напроксеном, клопидогрелом или эноксапарином не влияет на биодоступность и фармакокинетику ривароксабана.
Не наблюдалось никакого клинически значимого фармакокинетического или фармакодинамического взаимодействия при совместном применении Ксарелто® и 500 мг ацетилсалициловой кислоты.
Передозировка
Сообщалось о редких случаях передозировки при приеме ривароксабана до 600 мг без развития кровотечений или других нежелательных реакций. Вследствие ограниченного всасывания ожидается эффект насыщения без дальнейшего повышения среднего содержания ривароксабана в плазме при гипертерапевтических дозах (50 мг или выше).
Лечение: специфический антидот ривароксабана неизвестен. В случае передозировки для снижения всасывания ривароксабана можно использовать активированный уголь. Учитывая интенсивное связывание с белками плазмы крови, ожидается, что ривароксабан не будет выводиться при проведении диализа.
Лечение кровотечений
При возникновении осложнения в виде кровотечения, следующий прием препарата должен быть отложен или лечение должно быть отменено, в зависимости от ситуации. Т1/2 ривароксабана составляет приблизительно 5-13 ч. Лечение следует подбирать индивидуально, в соответствии с тяжестью и локализацией кровотечения.
При необходимости можно применять соответствующее симптоматическое лечение, такое как механическая компрессия (например, при тяжелых носовых кровотечениях), хирургический гемостаз с процедурами контроля кровотечения, восполнение объема жидкости и гемодинамическая поддержка, применение препаратов крови (эритроцитарная масса или свежезамороженная плазма, в зависимости от сопутствующей анемии или коагулопатии) или тромбоцитов.
Если перечисленные выше мероприятия не приводят к устранению кровотечения, может быть назначен специфический прокоагулянт, например, концентрат протромбинового комплекса, концентрат активированного протромбинового комплекса или рекомбинантный фактор VIIa (rf VIIa). Однако в настоящее время опыт применения этих препаратов при лечении пациентов, получающих ривароксабан, очень ограничен.
Ожидается, что протамина сульфат и витамин К не будут оказывать влияния на противосвертывающую активность ривароксабана.
Имеется ограниченный опыт применения транексамовой кислоты и отсутствует опыт применения аминокапроновой кислоты и апротинина у пациентов, получающих Ксарелто®. Научное обоснование целесообразности или опыт использования системного гемостатического препарата десмопрессин у пациентов, получающих Ксарелто®, отсутствует.
Влияние на способность к вождению автотранспорта и управлению механизмами
При применении препарата Ксарелто® отмечались случаи обмороков и головокружения, которые могут влиять на способность управления транспортными средствами или другими механизмами. Пациентам, у которых возникают такие неблагоприятные реакции, не следует управлять транспортными средствами или другими механизмами.
Список литературы (источники):
- Государственный реестр лекарственных средств
- Анатомо-терапевтическо-химическая классификация (ATX)
- Международная классификация болезней (МКБ-10)
- Официальная инструкция от производителя
Описание препарата Ксарелто® (таблетки, покрытые пленочной оболочкой, 2.5 мг) основано на официальной инструкции, утверждено компанией-производителем в 2020 году
Дата согласования: 02.07.2020
Особые отметки:
Содержание
- Фотографии упаковок
- Действующее вещество
- ATX
- Фармакологическая группа
- Нозологическая классификация (МКБ-10)
- Состав
- Описание лекарственной формы
- Фармакологическое действие
- Фармакодинамика
- Фармакокинетика
- Показания
- Противопоказания
- Применение при беременности и кормлении грудью
- Способ применения и дозы
- Побочные действия
- Взаимодействие
- Передозировка
- Особые указания
- Форма выпуска
- Производитель
- Условия отпуска из аптек
- Условия хранения
- Срок годности
- Аналоги (синонимы) препарата Ксарелто®
- Заказ в аптеках Москвы
Фотографии упаковок
02.07.2020
Действующее вещество
ATX
Фармакологическая группа
Состав
| Таблетки, покрытые пленочной оболочкой | 1 табл. |
| действующее вещество: | |
| ривароксабан микронизированный | 2,50 мг |
| вспомогательные вещества: целлюлоза микрокристаллическая — 40,00 мг; кроскармеллоза натрия — 3,00 мг; гипромеллоза 5сP (гидроксипропилметилцеллюлоза 2910) — 3,00 мг; лактозы моногидрат — 35,70 мг; магния стеарат — 0,60 мг; натрия лаурилсульфат — 0,20 мг | |
| оболочка пленочная: краситель железа оксид желтый — 0,015 мг; гипромеллоза 15сP (гидроксипропилметилцеллюлоза 2910) — 1,500 мг; макрогол 3350 (полиэтиленгликоль (3350) — 0,500 мг; титана диоксид — 0,485 мг |
Описание лекарственной формы
Круглые двояковыпуклые таблетки, покрытые пленочной оболочкой светло-желтого цвета. На одной стороне методом выдавливания нанесен треугольник с обозначением дозировки «2,5», на другой стороне — логотип компании Байер в виде креста.
Фармакологическое действие
Фармакодинамика
Механизм действия. Ривароксабан — высокоселективный прямой ингибитор фактора Ха, обладающий высокой биодоступностью при приеме внутрь.
Активация фактора X с образованием фактора Ха через внутренний и внешний пути свертывания играет центральную роль в коагуляционном каскаде. Фактор Ха является компонентом формирующегося протромбиназного комплекса, действие которого приводит к превращению протромбина в тромбин. В результате эти реакции приводят к формированию фибринового тромба и активации тромбоцитов тромбином. Одна молекула фактора Ха катализирует образование более 1000 молекул тромбина, что получило название «тромбинового взрыва». Скорость реакции связанного в протромбиназе фактора Ха увеличивается в 300000 раз по сравнению с таковой свободного фактора Ха, что обеспечивает резкий скачок в уровне тромбина. Селективные ингибиторы фактора Ха могут остановить «тромбиновый взрыв». Таким образом, ривароксабан оказывает влияние на результаты некоторых специфических или общих лабораторных исследований, применяемых для оценки свертывающих систем.
Фармакодинамические эффекты. У человека наблюдается дозозависимое ингибирование фактора Ха. Ривароксабан оказывает дозозависимое влияние на изменение протромбинового времени (ПВ), которое тесно коррелирует с концентрацией ривароксабана в плазме крови (коэффициент корреляции 0,98), если для анализа используется набор Neoplastin. При использовании других реактивов результаты будут отличаться.
ПВ следует измерять в секундах, поскольку международное нормализованное отношение (MHO) откалибровано и сертифицировано только для производных кумарина и не может применяться для других антикоагулянтов. У пациентов, которым проводятся большие ортопедические операции, 5/95-процентили значений для ПВ (Neoplastin) через 2–4 часа после приема таблетки (т.е. на максимуме эффекта) варьируют от 13 до 25 секунд.
Также ривароксабан дозозависимо увеличивает активированное частичное тромбопластиновое время (АЧТВ) и результат HepTest; однако эти параметры не рекомендуется использовать для оценки фармакодинамических эффектов ривароксабана.
В период лечения препаратом Ксарелто® проводить мониторинг параметров свертывания крови не требуется. Однако если для этого есть клиническое обоснование, концентрация ривароксабана может быть измерена при помощи калиброванного количественного теста антифактора Xa.
У здоровых мужчин и женщин старше 50 лет удлинения интервала QT ЭКГ под влиянием ривароксабана не наблюдалось.
Фармакокинетика
Всасывание и биодоступность. Ривароксабан быстро всасывается; максимальная концентрация (Cmax) достигается через 2–4 часа после приема таблетки.
После приема внутрь ривароксабан всасывается почти полностью, и его биодоступность при приеме таблеток 2,5 мг высокая (80–100%) вне зависимости от приема пищи. Прием пищи не оказывает влияние на площадь под кривой «концентрация — время» (AUC) и Cmax при приеме дозы 10 мг. Таблетки Ксарелто® в дозировке 2,5 мг могут приниматься как вместе с пищей, так и натощак (см. «Способ применения и дозы»).
Фармакокинетика ривароксабана характеризуется умеренной межиндивидуальной вариабельностью, коэффициент вариабельности (Cv%) составляет от 30 до 40%.
Всасывание ривароксабана зависит от места высвобождения в желудночно-кишечном тракте (ЖКТ). Снижение AUC и Cmax на 29% и 56% соответственно, в сравнении с приемом целой таблетки, наблюдалось при введении гранулята ривароксабана в проксимальный отдел тонкой кишки. Экспозиция препарата также уменьшается при его введении в дистальный отдел тонкой кишки или восходящую ободочную кишку. Следует избегать введения ривароксабана в ЖКТ дистальнее желудка, поскольку это может повлечь снижение всасывания и, соответственно, экспозиции препарата.
Биодоступность (AUC и Cmax) ривароксабана 20 мг при приеме целой таблетки сопоставима с биодоступностью препарата, принятого внутрь в виде измельченной таблетки (в смеси с яблочным пюре или суспендированной в воде), а также с биодоступностью препарата при введении через желудочный зонд с последующим приемом жидкого питания. Учитывая предсказуемый дозозависимый фармакокинетический профиль ривароксабана, результаты данного исследования биодоступности применимы также и к более низким дозам.
Распределение. Ривароксабан имеет высокую степень связывания с белками плазмы крови, она составляет приблизительно 92–95%, в основном ривароксабан связывается с сывороточным альбумином. Препарат имеет средний объем распределения, он составляет приблизительно 50 л.
Метаболизм и выведение. При приеме внутрь приблизительно 2/3 от полученной дозы ривароксабана метаболизируется и выводится почками и через кишечник в равных соотношениях. Оставшаяся треть полученной дозы выводится посредством прямой почечной экскреции в неизмененном виде, главным образом за счет активной почечной секреции.
Ривароксабан метаболизируется посредством изоферментов CYP3A4, CYP2J2, а также при помощи механизмов, независимых от системы цитохромов. Основными участками биотрансформации являются окисление морфолиновой группы и гидролиз амидных связей.
Согласно данным, полученным in vitro, ривароксабан является субстратом для белков-переносчиков Р-гликопротеина (P-gp) и белка устойчивости рака молочной железы (BCRP).
Неизмененный ривароксабан является единственным активным соединением в плазме крови, основные или активные циркулирующие метаболиты в плазме не обнаружены. Ривароксабан, системный клиренс которого составляет приблизительно 10 л/ч, может быть отнесен к лекарственным веществам с низким клиренсом. При выведении ривароксабана из плазмы конечный период полувыведения (T1/2) составляет от 5 до 9 часов у молодых пациентов и от 11 до 13 часов — у пожилых пациентов.
Пол/пожилой возраст (старше 65 лет). У пожилых пациентов концентрации ривароксабана в плазме крови выше, чем у молодых пациентов; среднее значение AUC приблизительно в 1,5 раза превышает соответствующие значения у молодых пациентов, главным образом вследствие кажущегося снижения общего и почечного клиренса (см. «Способ применения и дозы»). У мужчин и женщин клинически значимых различий фармакокинетики не обнаружено (см. «Способ применения и дозы»).
Масса тела. Слишком малая или большая масса тела (менее 50 и более 120 кг) лишь незначительно влияет на концентрацию ривароксабана в плазме крови (различие составляет менее 25%) (см. «Способ применения и дозы»).
Детский и подростковый возраст (с рождения до 18 лет). Данные по этой возрастной категории отсутствуют (см. «Способ применения и дозы»).
Межэтнические различия. Клинически значимых различий фармакокинетики и фармакодинамики у пациентов европеоидной, афроамериканской, латиноамериканской, японской или китайской этнической принадлежности не наблюдалось (см. «Способ применения и дозы»).
Нарушение функции печени. Влияние печеночной недостаточности на фармакокинетику ривароксабана изучалось у больных, распределенных в соответствии с классификацией Чайлд-Пью (согласно стандартным процедурам в клинических исследованиях). Классификация Чайлд-Пью позволяет оценить прогноз для пациента с хроническими заболеваниями печени, главным образом циррозом. Для пациентов, которым планируется проведение антикоагулянтной терапии, наиболее важным следствием нарушения функции печени является уменьшение синтеза факторов свертывания крови в печени. Так как этот показатель соответствует только одному из пяти клинических/биохимических критериев, составляющих классификацию Чайлд-Пью, риск развития кровотечения не совсем четко коррелирует с данной классификацией. Вопрос о лечении подобных пациентов антикоагулянтами должен решаться независимо от класса по классификации Чайлд-Пью.
Ривароксабан противопоказан пациентам с заболеваниями печени, протекающими с коагулопатией, обусловливающей клинически значимый риск развития кровотечения.
У пациентов с циррозом печени и легкой степенью печеночной недостаточности (класс А по Чайлд-Пью) фармакокинетика ривароксабана лишь незначительно отличалась от соответствующих показателей в контрольной группе здоровых добровольцев (в среднем отмечалось увеличение AUC ривароксабана в 1,2 раза). Значимые различия фармакодинамических свойств между группами отсутствовали.
У пациентов с циррозом печени и печеночной недостаточностью средней степени тяжести (класс В по Чайлд-Пью) средняя AUC ривароксабана была значительно повышена (в 2,3 раза) по сравнению со здоровыми добровольцами вследствие значительно сниженного клиренса лекарственного вещества, что указывает на серьезное заболевание печени. Подавление активности фактора Ха было выражено сильнее (в 2,6 раза), чем у здоровых добровольцев. ПВ также в 2,1 раза превышало показатели у здоровых добровольцев. При помощи измерения ПВ оценивается внешний путь коагуляции, включающий факторы свертывания VII, X, V, II и I, которые синтезируются в печени. Пациенты со среднетяжелой печеночной недостаточностью более чувствительны к ривароксабану, что является следствием более тесной взаимосвязи фармакодинамических эффектов и фармакокинетических параметров, особенно между концентрацией и ПВ.
Данные по пациентам с печеночной недостаточностью класса С по классификации Чайлд-Пью отсутствуют.
Нарушение функции почек. У пациентов с почечной недостаточностью наблюдалось увеличение AUC ривароксабана, обратно пропорциональное степени снижения почечной функции, которая оценивалась по клиренсу креатинина (Cl креатинина).
У пациентов с легкой (Cl креатинина 50–80 мл/мин), средней (Cl креатинина 30–50 мл/мин) или тяжелой степенью нарушения функции почек (Cl креатинина 15–29 мл/мин) наблюдалось 1,4-; 1,5- и 1,6-кратное увеличение концентраций ривароксабана в плазме крови (AUC) соответственно по сравнению со здоровыми добровольцами (см. «Способ применения и дозы», «Особые указания», С ОСТОРОЖНОСТЬЮ).
Соответствующее увеличение фармакодинамических эффектов было более выраженным.
У пациентов с легкой, средней и тяжелой степенью нарушения функции почек общее подавление активности фактора Ха увеличивалось в 1,5; 1,9 и 2 раза по сравнению со здоровыми добровольцами; ПВ вследствие действия фактора Ха также удлинялось в 1,3; 2,2 и 2,4 раза соответственно.
Данные о применении препарата Ксарелто® у пациентов с Cl креатинина 15–29 мл/мин ограничены, в связи с чем следует соблюдать осторожность при применении препарата у данной категории пациентов.
Данные о применении препарата Ксарелто® у пациентов с Cl креатинина <15 мл/мин отсутствуют, в связи с чем не рекомендуется применять препарат у данной категории пациентов (см. «Способ применения и дозы», «Особые указания», С ОСТОРОЖНОСТЬЮ).
В связи с основным заболеванием пациенты с тяжелой степенью нарушения функции почек подвержены повышенному риску развития кровотечений и тромбозов.
Показания
- профилактика смерти вследствие сердечно-сосудистых причин, инфаркта миокарда и тромбоза стента у пациентов после острого коронарного синдрома (ОКС), протекавшего с повышением кардиоспецифических биомаркеров, в комбинированной терапии с ацетилсалициловой кислотой или ацетилсалициловой кислотой и тиенопиридинами (клопидогрел или тиклопидин);
- профилактика инсульта, инфаркта миокарда и смерти вследствие сердечно-сосудистых причин, а также профилактика острой ишемии конечностей и общей смертности у пациентов с ишемической болезнью сердца (ИБС) или заболеванием периферических артерий (ЗПА) в комбинированной терапии с ацетилсалициловой кислотой.
Противопоказания
- повышенная чувствительность к ривароксабану или любому вспомогательному веществу, входящему в состав препарата;
- клинически значимые активные кровотечения (например, внутричерепное кровоизлияние, желудочно-кишечное кровотечение);
- заболевания печени, протекающие с коагулопатией, ведущей к клинически значимому риску развития кровотечения, в т.ч. цирроз печени и нарушения функции печени класса В и С по классификации Чайлд-Пью (см. «Фармакокинетика»);
- беременность (см. «Применение при беременности и кормлении грудью»);
- период грудного вскармливания (см. «Применение при беременности и кормлении грудью»);
- детский и подростковый возраст до 18 лет (эффективность и безопасность для пациентов данной возрастной группы не установлены).
- тяжелая степень нарушения функции почек (Cl креатинина <15 мл/мин) (клинические данные о применении ривароксабана у данной категории пациентов отсутствуют);
- лечение острого коронарного синдрома (ОКС) при помощи антиагрегантов у пациентов, перенесших инсульт или транзиторную ишемическую атаку (ТИА);
- сопутствующая терапия какими-либо другими антикоагулянтами, в т.ч. нефракционированным гепарином, низкомолекулярными гепаринами (в т.ч. эноксапарин, далтепарин), производными гепарина (в т.ч. фондапаринукс), пероральными антикоагулянтами (в т.ч. варфарин, апиксабан, дабигатран), кроме случаев перехода с или на ривароксабан (см. «Способ применения и дозы») или при применении нефракционированного гепарина в дозах, необходимых для обеспечения функционирования центрального венозного или артериального катетера;
- наследственная непереносимость лактозы или галактозы (например, врожденный дефицит лактазы или глюкозо-галактозная мальабсорбция) (в состав препарата входит лактоза).
С ОСТОРОЖНОСТЬЮ
- лечение пациентов с повышенным риском кровотечения (в т.ч. при врожденной или приобретенной склонности к кровоточивости, неконтролируемой тяжелой артериальной гипертонии, язвенной болезни желудка и двенадцатиперстной кишки в стадии обострения, недавно перенесенной острой язве желудка и двенадцатиперстной кишки, сосудистой ретинопатии, недавно перенесенном внутричерепном или внутримозговом кровоизлиянии, при наличии известных аномалий сосудов спинного или головного мозга, после недавно перенесенной операции на головном, спинном мозге или глазах, при наличии бронхоэктазов или легочном кровотечении в анамнезе);
- лечение пациентов со средней степенью нарушения функции почек (30–49 мл/мин), получающих одновременно препараты, повышающие концентрацию ривароксабана в плазме крови (см. «Взаимодействие»);
- лечение пациентов с тяжелой степенью нарушения функции почек (Cl креатинина 15–29 мл/мин) (см. «Особые указания»);
- пациенты, получающие одновременно лекарственные препараты, влияющие на гемостаз, в т.ч. нестероидные противовоспалительные препараты (НПВП), антиагреганты или другие антитромботические средства или селективные ингибиторы обратного захвата серотонина (СИОЗС) и селективные ингибиторы обратного захвата серотонина и норэпинефрина (СИОЗСН).
Ривароксабан не рекомендуется к применению у пациентов, получающих системное лечение противогрибковыми препаратами азоловой группы (в т.ч. кетоконазол, итраконазол, вориконазол и позаконазол) или ингибиторами протеазы ВИЧ (в т.ч. ритонавир) (см. «Взаимодействие», «Особые указания»).
Пациенты с тяжелой степенью нарушения функции почек (Cl креатинина 15–29 мл/мин) или повышенным риском развития кровотечения и пациенты, получающие сопутствующее системное лечение противогрибковыми препаратами азоловой группы или ингибиторами протеазы ВИЧ, после начала лечения должны находиться под пристальным контролем для своевременного обнаружения осложнений в форме кровотечения.
Применение при беременности и кормлении грудью
Беременность. Безопасность и эффективность применения ривароксабана у беременных женщин не установлены. Данные, полученные на экспериментальных животных, показали выраженную токсичность ривароксабана для материнского организма, связанную с фармакологическим действием препарата (например, осложнения в форме кровоизлияний) и приводящую к репродуктивной токсичности. Первичного тератогенного потенциала не обнаружено.
Вследствие возможного риска развития кровотечения и способности проникать через плаценту ривароксабан противопоказан при беременности (см. «Противопоказания»).
Женщинам с сохраненной репродуктивной способностью следует использовать эффективные методы контрацепции в период лечения ривароксабаном.
Грудное вскармливание. Данные о применении препарата Ксарелто® для лечения женщин в период грудного вскармливания отсутствуют. Данные, полученные на экспериментальных животных, показывают, что ривароксабан выделяется с грудным молоком. Препарат Ксарелто® может применяться только после прекращения грудного вскармливания (см. «Противопоказания»).
Способ применения и дозы
Внутрь, по 1 таблетке (1 табл.) 2 раза в день, независимо от приема пищи.
Профилактика смерти вследствие сердечно-сосудистых причин, инфаркта миокарда и тромбоза стента у пациентов после ОКС. После ОКС рекомендуемая доза препарата Ксарелто® 2,5 мг составляет 1 табл. 2 раза в день. Пациентам также необходимо принимать суточную дозу ацетилсалициловой кислоты 75–100 мг или суточную дозу ацетилсалициловой кислоты 75–100 мг в сочетании с суточной дозой клопидогрела 75 мг или стандартной суточной дозой тиклопидина.
Проводимое лечение должно регулярно оцениваться с точки зрения соблюдения баланса между риском развития ишемических событий и риском развития кровотечения. Продолжительность лечения составляет 12 мес. Лечение может быть продлено до 24 мес для отдельных пациентов, поскольку данные о лечении такой длительности ограничены.
Лечение препаратом Ксарелто® 2,5 мг следует начинать как можно раньше после стабилизации пациента в ходе текущего ОКС (включая процедуры реваскуляризации). Лечение препаратом Ксарелто® следует начинать минимум через 24 ч после госпитализации. Прием препарата Ксарелто® 2,5 мг следует начинать тогда, когда парентеральное введение антикоагулянтов обычно прекращается.
Профилактика инсульта, инфаркта миокарда и смерти вследствие сердечно-сосудистых причин, а также профилактика острой ишемии конечностей и общей смертности у пациентов с ИБС или ЗПА. Рекомендуемый режим дозирования для профилактики сосудистых событий у пациентов с ИБС или ЗПА составляет по 1 табл. препарата Ксарелто® 2,5 мг 2 раза в день в комбинации с суточной дозой ацетилсалициловой кислоты 75–100 мг. Лечение препаратом Ксарелто® 2,5 мг должно быть долгосрочным при условии, что получаемая польза превышает имеющиеся риски. У пациентов с острым тромботическим явлением или необходимостью вмешательства на сосудах, которым требуется двойная антитромбоцитарная терапия, следует оценить необходимость продолжения приема препарата Ксарелто® 2,5 мг 2 раза в день в зависимости от типа тромботического явления или процедуры, а также вида антитромбоцитарной терапии. Безопасность и эффективность препарата Ксарелто® 2,5 мг при приеме 2 раза в день в комбинации с ацетилсалициловой кислотой и клопидогрелем или тиклопидином были изучены только у пациентов, недавно перенесших ОКС. Применение двойной антитромбоцитарной терапии в комбинации с приемом препарата Ксарелто® 2,5 мг 2 раза в день у пациентов с ИБС или ЗПА не изучалось. Пациентам, которым диагностировали ИБС или ЗПА, лечение препаратом Ксарелто® 2,5 мг 2 раза в день в комбинации с ацетилсалициловой кислотой 75–100 мг 1 раз в день может быть начато в любое время.
Если доза пропущена, пациент должен продолжить прием препарата Ксарелто® 2,5 мг в обычной дозе, т.е. в следующий запланированный в соответствии с рекомендациями прием.
Если пациент не способен проглотить таблетку целиком, таблетка Ксарелто® может быть измельчена или смешана с водой или жидким питанием, например яблочным пюре, непосредственно перед приемом. Измельченная таблетка Ксарелто® может быть введена через желудочный зонд. Положение зонда в ЖКТ необходимо дополнительно согласовывать с врачом перед приемом Ксарелто®. Измельченную таблетку следует вводить через желудочный зонд в небольшом количестве воды, после чего необходимо ввести небольшое количество воды для того, чтобы смыть остатки препарата со стенок зонда (см. «Фармакокинетика»).
Дополнительная информация для особых групп пациентов
Пациенты с нарушением функции печени. Препарат Ксарелто® противопоказан пациентам с заболеваниями печени, протекающими с коагулопатией, ведущей к клинически значимому риску развития кровотечения (см. «Противопоказания»).
Пациентам с другими заболеваниями печени коррекция дозы не требуется (см. «Фармакокинетика»).
Ограниченные клинические данные, полученные у пациентов с умеренным нарушением функций печени (класс В по Чайльд-Пью), указывают на значительное увеличение фармакологической активности. Для пациентов с тяжелым нарушением функций печени (класс С по Чайльд-Пью) клинические данные отсутствуют (см. «Противопоказания», «Фармакокинетика»).
Пациенты с нарушением функции почек. Коррекция дозы не требуется, если препарат Ксарелто® применяется у пациентов с нарушением функции почек легкой (Cl креатинина 50–80 мл/мин) или средней (Cl креатинина 30–49 мл/мин) степени тяжести (см. «Фармакокинетика»).
Ограниченные клинические данные, полученные у пациентов с тяжелым нарушением функции почек (Cl креатинина 15–29 мл/мин), указывают на то, что концентрация ривароксабана в плазме крови в данной популяции пациентов значительно повышена. Поэтому у таких пациентов Ксарелто® необходимо использовать с осторожностью (см. «Особые указания», «Фармакокинетика»).
Применение препарата Ксарелто® не рекомендовано у пациентов с Cl креатинина <15 мл/мин (см. «Противопоказания»).
Переход с терапии антагонистами витамина К (АВК) на терапию препаратом Ксарелто®
При переходе пациентов с АВК на препарат Ксарелто® значения MHO будут ошибочно завышенными после приема препарата Ксарелто®. MHO не подходит для определения антикоагулянтной активности препарата Ксарелто® и поэтому не должно использоваться с этой целью (см. «Взаимодействие»).
Переход с терапии препаратом Ксарелто® на терапию АВК
Существует возможность возникновения недостаточного антикоагулянтного эффекта при переходе с терапии препаратом Ксарелто® на терапию АВК. В связи с этим необходимо обеспечить непрерывный достаточный антикоагулянтный эффект во время подобного перехода с помощью альтернативных антикоагулянтов. Следует отметить,что при переходе с препарата Ксарелто® на терапию АВК препарат Ксарелто® может способствовать повышению МНО.
У пациентов, которые переходят с терапии препаратом Ксарелто® на терапию АВК, последние следует принимать непрерывно до тех пор, пока значение MHO не составит ≥2,0. В первые два дня переходного периода АВК следует применять в стандартных дозах, адаптируя впоследствии дозу АВК в соответствии со значением MHO. Так как пациенты в этот период получают одновременно и препарат Ксарелто®, и АВК, MHO следует оценивать не ранее чем через 24 часа (после первой дозы, но до следующего приема препарата Ксарелто®). Таким образом, после прекращения применения препарата Ксарелто® MHO в качестве надежной оценки терапевтического эффекта АВК может использоваться не ранее чем через 24 часа после последнего приема препарата Ксарелто® (см. «Взаимодействие», «Способ применения и дозы»).
Переход с терапии парентеральными антикоагулянтами на терапию препаратом Ксарелто®
Для пациентов, получающих парентеральные антикоагулянты, применение Ксарелто® следует начинать за 0–2 часа до времени следующего планового парентерального введения препарата (в т.ч. низкомолекулярный гепарин) или в момент прекращения непрерывного парентерального введения препарата (в т.ч. при внутривенном введение нефракционированного гепарина).
Переход с терапии препаратом Ксарелто® на терапию парентеральными антикоагулянтами
Следует отменить препарат Ксарелто® и ввести первую дозу парентерального антикоагулянта в то время, когда нужно будет принимать следующую дозу препарата Ксарелто®.
Дети и подростки (с рождения до 18 лет). Безопасность и эффективность применения у детей и подростков до 18 лет не установлены.
Пожилой возраст. Коррекция дозы в зависимости от возраста не требуется (см. «Фармакокинетика»).
Пол. Коррекция дозы в зависимости от пола не требуется (см. «Фармакокинетика»).
Масса тела. Коррекция дозы в зависимости от массы тела не требуется (см. «Фармакокинетика»).
Этническая принадлежность. Коррекция дозы в зависимости от этнической принадлежности не требуется (см. «Фармакокинетика»).
Побочные действия
Реклама: ООО «РЛС-Патент», ИНН 5044031277
Безопасность препарата Ксарелто® оценивалась в тринадцати исследованиях III фазы, включавших 53103 пациентов, принимавших препарат Ксарелто®.
Таблица 1
Число пациентов, участвовавших в исследовании и принявших как минимум 1 дозу ривароксабана, суммарная суточная доза и максимальная продолжительность лечения в клинических исследованиях III фазы с использованием препарата Ксарелто®.
| Терапевтическая область | Число пациентов, получивших по меньшей мере 1 дозу ривароксабана | Суммарная суточная доза, мг | Максимальная продолжительность лечения |
| Профилактика венозной тромбоэмболии (ВТЭ) у пациентов, перенесших плановую операцию по замене тазобедренного или коленного сустава | 6097 | 10 | 39 дней |
| Профилактика ВТЭ у госпитализированных по медицинским показаниям пациентов | 3997 | 10 | 39 дней |
| Лечение ТГВ, ТЭЛА и профилактика рецидивов ТГВ, ТЭЛА | 6790 | День 1–21 — 30 мг; начиная с 22 дня — 20 мг; после минимум 6 мес терапии — 10 или 20 мг | 21 месяц |
| Профилактика инсульта и системной тромбоэмболии у пациентов с фибрилляцией предсердий неклапанного происхождения | 7750 | 20 | 41 месяц |
| Профилактика атеротромботических событий у пациентов после ОКС | 10225 | 5 или 10 мг соответственно, совместно с ацетилсалициловой кислотой или ацетилсалициловой кислотой с клопидогрелом или тиклопидином | 31 месяц |
| Профилактика инсульта, инфаркта миокарда и смерти вследствие сердечно-сосудистых причин, а также для профилактики острой ишемии конечностей и общей смертности у пациентов с ИБС или ЗПА | 18224 | 5 мг в комбинации с ацетилсалициловой кислотой 100 мг или 10 мг в монотерапии | 47 месяцев |
Таблица 2
Частота возникновения кровотечений и анемии у пациентов, получавших препарат Ксарелто®, по результатам исследований III фазы
| Показания к применению | Любое кровотечение | Анемия |
| Профилактика ВТЭ у пациентов, перенесших плановую операцию по замене тазобедренного или коленного сустава | 6,8% пациентов | 5,9% пациентов |
| Профилактика ВТЭ у госпитализированных по медицинским показаниям пациентов | 12,6% пациентов | 2,1% пациентов |
| Лечение ТГВ, ТЭЛА и профилактика рецидивов ТГВ, ТЭЛА | 23% пациентов | 1,6% пациентов |
| Профилактика инсульта и системной тромбоэмболии у пациентов с фибрилляцией предсердий неклапанного происхождения | 28 событий на 100 пациенто-лет | 2,5 события на 100 пациенто-лет |
| Профилактика атеротромботических осложнений у пациентов после ОКС | 22 события на 100 пациенто-лет | 1,4 события на 100 пациенто-лет |
| Профилактика инсульта, инфаркта миокарда и смерти вследствие сердечно-сосудистых причин, а также для профилактики острой ишемии конечностей и общей смертности у пациентов с ИБС или ЗПА | 6,7 события на 100 пациенто-лет | 0,15 события на 100 пациенто-лет* |
*При сборе данных о нежелательных явлениях применялся предустановленный выборочный подход
Учитывая механизм действия, применение препарата Ксарелто® может быть связано с повышением риска развития скрытых или явных кровотечений из любых тканей и органов, которые могут привести к развитию постгеморрагической анемии. Риск развития кровотечения может увеличиваться у пациентов с тяжелой неконтролируемой артериальной гипертензией и/или при совместном применении с препаратами, влияющими на гемостаз (см. С ОСТОРОЖНОСТЬЮ).
Признаки, симптомы и тяжесть (включая возможный летальный исход) будут варьировать в зависимости от источника и степени или выраженности кровотечения и/или анемии (см. «Передозировка»).
Геморрагические осложнения могут проявляться в виде слабости, бледности, головокружения, головной боли или необъяснимых отеков, одышки или шока, развитие которого нельзя объяснить другими причинами. В некоторых случаях, как следствие анемии, наблюдаются симптомы ишемии миокарда, такие как боли в грудной клетке или стенокардия.
При применении препарата Ксарелто® регистрировались и такие известные осложнения, вторичные по отношению к тяжелым кровотечениям, как синдром повышенного субфасциального давления (компартмент-синдром) и почечная недостаточность вследствие гипоперфузии. Таким образом, при оценке состояния любого пациента, получающего антикоагулянты, следует учитывать возможность развития кровотечения.
Частота встречаемости нежелательных лекарственных реакций (НЛР) при использовании Ксарелто® приведена в таблице ниже. В рамках каждой группы, выделенной по частоте, нежелательные явления представлены в порядке уменьшения их серьезности. Частота встречаемости определяется как: очень часто (≥1/10); часто (≥1/100 до <1/10); нечасто (≥1/1000 до <1/100); редко (≥1/10000 до <1/1000).
Таблица 3
Все возникшие на фоне лечения нежелательные лекарственные реакции, зарегистрированные у пациентов в исследованиях III фазы (кумулятивные данные RECORD 1–4, ROCKET AF, J-ROCKET, MAGELLAN, ATLAS и EINSTEIN (DVT/PE/Extension/CHOICE и COMPASS*)
| Системно-органный класс (MedDRA — Медицинский словарь нормативно-правовой лексики версия 20.0) | Часто | Нечасто | Редко |
| Нарушения со стороны системы кроветворения и лимфатической системы | Анемия (включая соответствующие лабораторные показатели) | Тромбоцитоз (включая повышение количества тромбоцитов)А | − |
| Нарушения со стороны иммунной системы | − | Аллергическая реакция, аллергический дерматит | − |
| Нарушения со стороны нервной системы | Головокружение, головная боль | Внутримозговые и внутричерепные кровоизлияния, обморок | − |
| Нарушения со стороны органа зрения | Кровоизлияние в глаз (включая кровоизлияние в конъюнктиву) | − | − |
| Нарушения со стороны сердца | − | Тахикардия | − |
| Нарушения со стороны сосудов | Снижение артериального давления (АД), гематома | − | − |
| Нарушения со стороны дыхательной системы, органов грудной клетки и средостения | Носовое кровотечение, кровохарканье | − | − |
| Нарушения со стороны ЖКТ | Кровоточивость десен, желудочно-кишечное кровотечение (включая ректальное), боль в области ЖКТ и животе, диспепсия, тошнота, запорА, диарея, рвотаА | Сухость во рту | − |
| Нарушения со стороны печени и желчевыводящих путей | − | Нарушение функции печени | Желтуха |
| Нарушения со стороны кожи и подкожных тканей | Кожный зуд (включая нечастые случаи генерализованного зуда), сыпь, экхимоз, кожные и подкожные кровоизлияния | Крапивница | − |
| Нарушения со стороны скелетно-мышечной системы, соединительной ткани и костей | Боль в конечностяхА | Гемартроз | Кровоизлияние в мышцу |
| Нарушения со стороны почек и мочевыводящих путей | Кровотечение из урогенитального тракта (включая гематурию и меноррагиюВ), нарушение функции почек (включая повышение креатинина крови, повышение мочевины крови)А | − | − |
| Общие расстройства и нарушения в месте введения | ЛихорадкаА, периферический отек, снижение общей мышечной силы и тонуса (включая слабость и астению) | Ухудшение общего самочувствия (включая недомогание) | Локальный отекА |
| Лабораторные и инструментальные данные | Повышение активности печеночных трансаминаз | Повышение концентрации билирубина, повышение активности щелочной фосфотазы (ЩФ)А, повышение активности ЛДГА, повышение активности липазыА, повышение активности амилазыА повышение активности ГГТА | Повышение концентрации конъюгированного билирубина (с соответствующим повышением активности АЛТ или без него). |
| Травмы, отравления и осложнения после манипуляций | Кровотечение после медицинской манипуляции (включая послеоперационную анемию и кровотечение из раны), гематома | Выделение секрета из раныА | Сосудистая псевдоаневризмаС |
АНаблюдались преимущественно после больших ортопедических операций на нижних конечностях.
ВНаблюдались при лечении ВТЭ как очень частые у женщин в возрасте <55 лет.
СНаблюдались как нечастые в рамках профилактики осложнений при ОКС (после чрескожных вмешательств).
*Применялся предварительно заданный избирательный подход к сбору данных по нежелательным явлениям. Так как частота нежелательных лекарственных реакций не повысилась, и так как никаких новых НЛР идентифицировано не было, данные из исследования COMPASS не были включены для расчета частоты в данной таблице.
Наиболее частыми НЛР у пациентов, применявших препарат, являлись кровотечения. Наиболее частыми кровотечениями (≥4%) являлись носовое (5,9%) и желудочно-кишечное кровотечение (4,2%).
При проведении пострегистрационного мониторинга сообщалось о случаях приведенных ниже нежелательных реакций, развитие которых имело временную связь с приемом препарата Ксарелто®. Оценить частоту встречаемости таких нежелательных реакций в рамках пострегистрационного мониторинга не представляется возможным.
Нарушения со стороны иммунной системы: ангионевротический отек, аллергический отек. В рамках регистрационных клинических исследований (РКИ) III фазы такие нежелательные реакции были расценены как нечастые (≥1/1000 до <1/100).
Нарушения со стороны печени и желчевыводящих путей: холестаз, гепатит (включая гепатоцеллюлярное повреждение). В рамках РКИ III фазы такие нежелательные реакции были расценены как редкие (≥1/10000 до <1/1000).
Нарушения со стороны крови и лимфатической системы: тромбоцитопения. В рамках РКИ III фазы такие нежелательные реакции были расценены как нечастые (≥1/1000 до <1/100).
Взаимодействие
Фармакокинетические взаимодействия (ФКВ)
Ривароксабан в основном выводится с помощью опосредованного цитохромом Р450 (CYP3А4, CYP2J2) метаболизма в печени и почечной экскрецией неизмененного препарата с участием Р-gp и системы BCRP.
Следует соблюдать осторожность при одновременном применении ривароксабана с дронедароном в связи с ограниченностью клинических данных о совместном применении
Ингибирование CYP. Ривароксабан не ингибирует CYP3А4 или любые другие основные изоформы CYP.
Индукция CYP. Ривароксабан не индуцирует CYP3А4 или любые другие основные изоформы CYP.
Влияние на ривароксабан. Одновременное применение ривароксабана с мощными ингибиторами CYP3А4 и P-gp может привести к снижению печеночного и почечного клиренса и таким образом значительно увеличить системное воздействие.
Одновременное применение ривароксабана с азоловым противогрибковым препаратом кетоконазолом (400 мг 1 раз в день), мощным ингибитором CYP3А4 и Р-gp, приводило к увеличению средней равновесной AUC и средней Cmax ривароксабана в 2,6 и 1,7 раза, со значительным усилением фармакодинамических эффектов данного препарата.
Одновременное применение ривароксабана с ингибитором протеазы ВИЧ ритонавиром (600 мг 2 в день), мощным ингибитором CYP3А4 и P-gp, приводило к увеличению средней равновесной AUC и средней Cmax ривароксабана в 2,5 и 1,6 раза соответственно, со значительным усилением фармакодинамических эффектов данного препарата.
Поэтому ривароксабан не рекомендуется использовать у пациентов, получающих сопутствующее системное лечение азоловыми противогрибковыми препаратами или ингибиторами протеазы ВИЧ (см. С ОСТОРОЖНОСТЬЮ, «Особые указания»).
Другие активные вещества, угнетающие хотя бы один из путей элиминации ривароксабана, опосредованный или CYP3А4, или P-gp, вероятно, в меньшей степени будут повышать концентрации ривароксабана в плазме крови.
Кларитромицин (500 мг 2 в день), который считается мощным ингибитором CYP3А4 и умеренным ингибитором P-gp, приводил к увеличению средней равновесной AUC и средней Cmax ривароксабана в 1,5 и 1,4 раза соответственно. Это увеличение, близкое к величине нормальной изменчивости AUC и Cmax, рассматривалось как клинически незначимое.
Эритромицин (500 мг 3 раза в день), который умеренно ингибирует CYP3А4 и P-gp, приводил к увеличению средней AUC и Cmax ривароксабана в 1,3 раза. Это увеличение, близкое к величине нормальной изменчивости AUC и Cmax, рассматривалось как клинически незначимое.
У пациентов с легкой степенью нарушения функции почек (Cl креатинина 50–80 мл/мин) эритромицин (500 мг 3 раза в день) вызывал увеличение значений AUC и Cmax в 1,8 и 1,6 раза соответственно по сравнению с пациентами с нормальной функцией почек, не получавших сопутствующей терапии. У пациентов со средней степенью нарушения функции почек (Cl креатинина 30–49 мл/мин) эритромицин вызывал увеличение значений AUC и Cmax в 2 и 1,6 раза соответственно по сравнению с пациентами с нормальной функцией почек, не получавших сопутствующей терапии (см. С ОСТОРОЖНОСТЬЮ).
Флуконазол (400 мг 1 раз в день), который считается умеренным ингибитором CYP3А4, приводил к увеличению средней AUC ривароксабана в 1,4 раза и увеличению средней Cmax в 1,3 раза. Это увеличение находилось в пределах величины нормальной изменчивости AUC и Cmax и рассматривалось как клинически незначимое (см. «Особые указания»).
Одновременное применение ривароксабана с мощным индуктором CYP3А4 и P-gp рифампицином приводило к уменьшению AUC ривароксабана в среднем приблизительно на 50%, с параллельным снижением его фармакодинамических эффектов. Одновременное использование ривароксабана с другими мощными индукторами CYP3А4 (в т.ч. фенитоин, карбамазепин, фенобарбитал или зверобой продырявленный) также может привести к снижению концентрации ривароксабана в плазме.
Мощные индукторы CYP3A4 необходимо применять с осторожностью у пациентов с ИБС, ЗПА или после ОКС, получающих препарат Ксарелто® 2,5 мг 2 раза в сутки.
Фармакодинамические взаимодействия (ФДВ)
После одновременного применения эноксапарина (40 мг однократно) с препаратом Ксарелто® (10 мг однократно) наблюдался суммационный эффект, связанный с подавляющим влиянием на активность фактора Ха без какого-либо дополнительного влияния на показатели свертывания (ПВ, АЧТВ). Эноксапарин не влияет на фармакокинетику ривароксабана (см. «Особые указания»).
Клопидогрел (насыщающая доза 300 мг, за которой следует поддерживающая доза 75 мг) не продемонстрировал ФКВ (с препаратом Ксарелто® в дозе 15 мг), однако было зарегистрировано значимое увеличение времени кровотечения в подгруппе пациентов, которое не коррелировало со степенью агрегации тромбоцитов, количеством рецепторов к Р-селектину или GPIIb/IIIa (см. «Особые указания»).
После одновременного применения препарата Ксарелто® (15 мг) и напроксена (500 мг) клинически значимого увеличения времени кровотечения не наблюдалось. Тем не менее могут встречаться пациенты с более выраженным фармакодинамическим ответом (см. «Особые указания»).
Следует соблюдать осторожность при одновременном применении ривароксабана с дронедароном в связи с ограниченностью клинических данных о совместном применении.
В связи с повышенным риском кровотечения необходимо соблюдать осторожность при совместном применении с любыми другими антикоагулянтами (см. «Противопоказания», С ОСТОРОЖНОСТЬЮ и «Особые указания»).
Необходимо соблюдать осторожность при совместном применении Ксарелто® с НПВП (включая ацетилсалициловую кислоту) и антиагрегантными средствами, поскольку применение этих препаратов обычно повышает риск развития кровотечения.
Переход пациентов с варфарина (MHO = от 2 до 3) на препарат Ксарелто® (20 мг) или с препарата Ксарелто® (20 мг) на варфарин (MHO = от 2 до 3) увеличивал ПВ/МНО (Neoplastin) больше, чем при простой суммации эффектов (отдельные значения MHO могут достигать 12), в то время как влияние на АЧТВ, подавление активности фактора Ха и влияние на эндогенный потенциал тромбина (ЭПТ) было аддитивным.
В случае необходимости исследования фармакодинамических эффектов препарата Ксарелто® во время переходного периода в качестве необходимых тестов, на которые не оказывает влияние варфарин, можно использовать определение активности антифактора Ха, протромбиназоиндуцированное время свертывания и НepTest.
Начиная с 4-го дня после прекращения применения варфарина все лабораторные показатели (в т.ч. ПВ, АЧТВ, ингибирование активности фактора Ха и ЭПТ) отражают только влияние препарата Ксарелто® (см. «Способ применения и дозы»).
Если необходимо исследовать фармакодинамические эффекты варфарина во время переходного периода, можно использовать значение MHO при Ctrought ривароксабана (через 24 часа после приема первой дозы ривароксабана), т.к. в данный момент времени ривароксабан практически не оказывает влияния на этот показатель.
Между варфарином и препаратом Ксарелто® — не было зарегистрировано никаких ФКВ.
Как и в случае применения других антикоагулянтов, необходимо соблюдать осторожность при совместном применении препарата Ксарелто® с СИОЗС и СИОЗСН, поскольку применение этих препаратов повышает риск кровотечения. Результаты клинических исследований продемонстрировали численное повышение больших и небольших клинически значимых кровотечений во всех группах лечения при совместном применении этих препаратов.
Продукты питания и молочные продукты. Препарат Ксарелто® можно принимать независимо от приема пищи (см. «Фармакокинетика»).
Взаимодействия отсутствуют. ФКВ ривароксабана и мидазолама (субстрат CYP3А4), дигоксина (субстрат P-gp) или аторвастатина (субстрат CYP3А4 и P-gp) отсутствуют.
Одновременное назначение ингибитора протонного насоса омепразола, антагониста Н2-гистаминовых рецепторов ранитидина, антацида гидроксида алюминия/гидроксида магния, напроксена, клопидогрела или эноксапарина не оказывает влияние на биодоступность и фармакокинетику ривароксабана.
Клинически значимых ФКВ и ФДВ при сочетанном приеме препарата Ксарелто® и ацетилсалициловой кислоты в дозе 500 мг выявлено не было.
Влияние на лабораторные показатели. Препарат Ксарелто® оказывает влияние на показатели свертываемости крови (ПВ, АЧТВ, HepTest) в связи со своим механизмом действия.
Передозировка
Были зарегистрированы редкие случаи передозировки до 600 мг без развития кровотечений или других нежелательных явлений. В связи с ограниченным всасыванием ожидается формирование плато концентрации без дальнейшего увеличения средней концентрации ривароксабана в плазме при применении супратерапевтических доз, равных 50 мг или выше.
Специфического антидота, противодействующего фармакодинамическим эффектам ривароксабана, не существует. В случае передозировки Ксарелто® можно использовать активированный уголь для уменьшения всасывания препарата. В связи со значительным связыванием с белками плазмы считается, что ривароксабан не будет выводиться с помощью гемодиализа.
Лечение кровотечений
Если у пациента, получающего ривароксабан, возникло осложнение в виде кровотечения, следующий прием препарата следует отложить или при необходимости вообще отменить лечение данным препаратом. T1/2 ривароксабана составляет приблизительно от 5 до 13 часов. Лечение должно быть индивидуальным, в зависимости от тяжести и локализации кровотечения. При необходимости можно использовать соответствующее симптоматическое лечение, такое как механическая компрессия (например, при тяжелых носовых кровотечениях), хирургический гемостаз с применением процедур контроля за продолжением кровотечения, инфузионная терапия и гемодинамическая поддержка, применение препаратов крови (эритроцитарная масса или свежезамороженная плазма, в зависимости от того, возникла анемия или коагулопатия) или тромбоцитов.
Если не представляется возможным контролировать кровотечение с помощью приведенных выше процедур, можно использовать введение специфических прокоагулянтных препаратов обратного действия, таких как концентрат протромбинового комплекса, концентрат активированного протромбинового комплекса или рекомбинантный фактор VIIa (rf VIIa). Однако в настоящее время опыт применения данных препаратов у пациентов, получающих препарат Ксарелто®, весьма ограничен.
Предполагается, что протамина сульфат и витамин К не будут оказывать влияние на антикоагулянтную активность ривароксабана.
Имеется ограниченный опыт применения транексамовой кислоты и отсутствует опыт применения аминокапроновой кислоты и апротинина у пациентов, получающих препарат Ксарелто®. Научное обоснование целесообразности или опыт применения системного гемостатического препарата десмопрессин у пациентов, получающих препарат Ксарелто®, отсутствует.
Особые указания
Применение сопутствующих препаратов
Ривароксабан не рекомендуется применять у пациентов, получающих сопутствующее системное лечение азоловыми противогрибковыми препаратами (в т.ч. кетоконазол) или ингибиторами ВИЧ-протеаз (в т.ч. ритонавир). Эти препараты являются сильными ингибиторами CYP3А4 и Р-gp. Таким образом, эти препараты могут повышать концентрацию ривароксабана в плазме крови до клинически значимых значений (в 2,6 раза в среднем), что может привести к повышенному риску развития кровотечений (см. «Взаимодействие»).
Однако азоловый противогрибковый препарат флуконазол, умеренный ингибитор CYP3A4, оказывает менее выраженное влияние на экспозицию ривароксабана и может применяться с ним одновременно (см. «Взаимодействие»).
Нарушение функции почек
Ривароксабан следует с осторожностью использовать у пациентов со средней степенью нарушения функции почек (Cl креатинина 30–49 мл/мин), получающих сопутствующие препараты, которые могут приводить к повышению концентрации ривароксабана в плазме (см. «Взаимодействие»).
У пациентов с тяжелой степенью нарушения функции почек (Cl креатинина <30 мл/мин) концентрация ривароксабана в плазме может быть значительно повышенной (в 1,6 раза в среднем), что может привести к повышенному риску развития кровотечения. Поэтому вследствие наличия указанного основного заболевания такие пациенты имеют повышенный риск развития как кровотечений, так и тромбозов. В связи с ограниченным количеством клинических данных, ривароксабан должен использоваться с осторожностью у пациентов с Cl креатинина 15–29 мл/мин.
Клинические данные о применении ривароксабана у пациентов с тяжелым нарушением функции почек (Cl креатинина <15 мл/мин) отсутствуют. Поэтому ривароксабан не рекомендуется к применению у таких пациентов (см. «Способ применения и дозы», «Фармакокинетика», «Фармакодинамика»).
За пациентами с тяжелым нарушением функции почек (Cl креатинина 15–29 мл/мин) или повышенным риском развития кровотечения, а также пациентами, получающими сопутствующее системное лечение азоловыми противогрибковыми препаратами или ингибиторами ВИЧ-протеаз, необходимо проводить тщательное наблюдение на предмет наличия признаков кровотечения после начала лечения.
Наблюдение может осуществляться путем проведения регулярного физикального обследования пациентов, тщательного контроля за состоянием дренажа послеоперационной раны, а также путем периодического определения гемоглобина (Hb).
Пациенты с инсультом или ТИА в анамнезе
Прием препарата Ксарелто® в дозе 2,5 мг 2 раза в сутки противопоказан у пациентов с ОКС, имеющих инсульт или ТИА в анамнезе. Было проведено исследование лишь нескольких пациентов с ОКС, имеющих в анамнезе инсульт или ТИА, но полученные ограниченные данные демонстрируют отсутствие клинической выгоды от лечения ривароксабаном у таких пациентов.
Пациенты с геморрагическим или лакунарным инсультом
Пациенты с ИБС или ЗПА с наличием в анамнезе геморрагического или лакунарного инсульта не изучались. Таким пациентам противопоказано лечение препаратом Ксарелто® 2,5 мг 2 раза в день в комбинации с ацетилсалициловой кислотой.
Пациенты с ишемическим нелакунарным инсультом
Пациенты с ИБС или ЗПА, у которых наблюдался ишемический нелакунарный инсульт в течение предшествующего месяца, не изучались. Таким пациентам противопоказано лечение препаратом Ксарелто® 2,5 мг 2 раза в день в комбинации с ацетилсалициловой кислотой в течение первого месяца после инсульта.
Риск кровотечения
Как и при приеме других антикоагулянтов необходимо тщательно наблюдать пациентов, принимающих препарат Ксарелто®, для выявления признаков кровотечения. В случае тяжелого кровотечения прием препарата Ксарелто® должен быть прекращен. В клинических исследованиях кровотечения из слизистых оболочек (а именно: кровотечение из носа, десен, желудочно-кишечного тракта, мочеполовой системы, включая аномальное вагинальное или усиленное менструальное кровотечение) и анемия наблюдались чаще при длительном лечении ривароксабаном в дополнение к монотерапии или двойной антитромбоцитарной терапии. Таким образом, в дополнение к надлежащему клиническому наблюдению, лабораторное исследование Hb/гематокрита может быть значимым для выявления скрытых кровотечений и количественной оценки клинической значимости явных кровотечений, которые будут сочтены допустимыми.
Препарат Ксарелто®, как и другие антитромботические средства, следует с осторожностью применять у пациентов с повышенным риском развития таких кровотечений, при:
— врожденных или приобретенных нарушениях свертывания;
— неконтролируемой тяжелой артериальной гипертензии;
— активной желудочно-кишечной патологии с язвообразованием;
— недавно перенесенной острой язве в ЖКТ;
— сосудистой ретинопатии;
— недавнем внутричерепном или внутримозговом кровоизлиянии;
— интраспинальных или интрацеребральных сосудистых аномалиях;
— недавно проведенной хирургической операции на головном, спинном мозге или офтальмологической операции;
— бронхоэктазах или эпизоде легочного кровотечения в анамнезе.
Следует соблюдать осторожность, если пациент одновременно получает лекарственные препараты, влияющие на гемостаз, такие как НПВП, ингибиторы агрегации тромбоцитов или другие антитромботические препараты или СИОЗС и СИОЗСН (см. «Взаимодействие»).
Пациенты, получающие препарат Ксарелто® в сочетании с ацетилсалициловой кислотой или препарат Ксарелто® в сочетании с ацетилсалициловой кислотой и клопидогрелом/тиклопидином, в качестве длительного сопутствующего лечения могут получать НПВП, только если положительные эффекты лечения оправдывают имеющийся риск развития кровотечения.
У пациентов с риском язвообразования в ЖКТ можно использовать соответствующее профилактическое лечение (см. «Взаимодействие»).
Любое необъяснимое снижение Hb или АД должно приводить к поиску источника кровотечения.
У пациентов после ОКС эффективность и безопасность препарата Ксарелто® 2,5 мг два раза в день были изучены в комбинации с антиагрегантным средством ацетилсалициловой кислотой или с ацетилсалициловой кислотой и клопидогрелом/тиклопидином. Применение в комбинированной терапии с другими антиагрегантными средствами (например, прасугрелом или тикагрелором) не было изучено, по этой причине не рекомендовано к применению.
Спинальная анестезия
При выполнении эпидуральной/спинальной анестезии или спинномозговой пункции у пациентов, получающих ингибиторы агрегации тромбоцитов с целью профилактики тромбоэмболических осложнений, существует риск развития эпидуральной или спинномозговой гематомы, которая может привести к длительному параличу.
Риск возникновения этих событий в дальнейшем повышается при применении постоянного эпидурального катетера или сопутствующей терапии лекарственными препаратами, влияющими на гемостаз. Травматичное выполнение эпидуральной или спинномозговой пункции или повторная пункция также могут повышать риск. Пациенты должны находиться под наблюдением для выявления признаков или симптомов неврологических нарушений (например, онемение или слабость ног, дисфункция кишечника или мочевого пузыря). При обнаружении неврологических расстройств необходима срочная диагностика и лечение.
Врач должен сопоставить потенциальную пользу и относительный риск перед проведением спинномозгового вмешательства у пациентов, получающих антикоагулянты, или которым планируется назначение антикоагулянтов с целью профилактики тромбозов.
Опыт клинического применения ривароксабана в дозировке 2,5 мг с ацетилсалициловой кислотой или с ацетилсалициловой кислотой и клопидогрелом или тиклопидином в описанных ситуациях отсутствует.
С целью снижения потенциального риска развития кровотечения, ассоциированного с одновременным применением ривароксабана и выполнением эпидуральной/спинальной анестезии или спинальной пункции, следует учитывать фармакокинетический профиль ривароксабана. Установку или удаление эпидурального катетера или люмбальную пункцию лучше проводить тогда, когда антикоагулянтный эффект ривароксабана оценивается как слабый (см. «Фармакокинетика»). Однако точное время для достижения достаточно низкого антикоагулянтного эффекта у каждого пациента неизвестно.
Следует обращать внимание на одновременное применение ингибиторов агрегации тромбоцитов и в случае необходимости прекратить их применение.
Хирургические операции и вмешательства
Если необходимо проведение инвазивной процедуры или хирургического вмешательства, прием препарата Ксарелто® 2,5 мг следует прекратить по крайней мере за 12 часов до вмешательства, если это возможно, и на основании клинической оценки врача.
Если у пациента, получающего ингибиторы агрегации тромбоцитов, которому проводится плановое оперативное вмешательство, отсутствует необходимость в антиагрегантном эффекте, применение ингибиторов агрегации тромбоцитов следует прекратить, как указано в инструкции по применению препарата, предоставляемой производителем.
Если процедуру нельзя отложить, необходимо провести сравнительную оценку повышенного риска развития кровотечения и необходимости срочного вмешательства.
Прием препарата Ксарелто® следует возобновить, как только это будет возможно после инвазивной процедуры или хирургического вмешательства, при условии, что клинические показатели будут позволять и будет достигнут адекватный гемостаз (см. «Фармакокинетика», Метаболизм и выведение).
Пациенты с искусственными клапанами сердца
Основываясь на данных рандомизированного контролируемого клинического исследования по сравнению терапии препаратом Ксарелто® и антитромбоцитарной терапии, применение препарата Ксарелто® не рекомендуется для профилактики тромбозов у пациентов, перенесших недавнюю транскатетерную замену аортального клапана.
Безопасность и эффективность применения препарата Ксарелто® не изучались у пациентов с какими-либо другими искусственными клапанами сердца или у пациентов после иных вмешательств на клапанах сердца, следовательно, нет данных, подтверждающих, что применение препарата Ксарелто® обеспечивает достаточный антикоагулянтный эффект у данных категорий пациентов.
Пациенты с высоким риском тройного позитивного антифосфолипидного синдрома
Применение препарата Ксарелто® не рекомендуется у пациентов, имеющих тромбозы в анамнезе, у которых диагностирован устойчивый тройной позитивный антифосфолипидный синдром (наличие волчаночного антикоагулянта, антител к кардиолипину и антител к бета-2-гликопротеину I), поскольку терапия ривароксабаном сопровождается повышенной частотой рецидивов тромботических событий в сравнении с терапией АВК).
Кожные реакции
При проведении постмаркетинговых наблюдений сообщалось о случаях возникновения синдрома Стивенса-Джонсона и токсического эпидермального некролиза. При первом появлении тяжелой кожной сыпи (например, при ее распространении, интенсификации и/или образовании волдырей) или наличии других симптомов гиперчувствительности, связанных с поражением слизистой оболочки, следует прекратить терапию препаратом Ксарелто®.
Женщины детородного возраста
Препарат Ксарелто® можно использовать у женщин детородного возраста только при условии применения эффективных методов контрацепции.
Удлинение интервала QT
На фоне лечения ривароксабаном удлинения интервала QT не наблюдалось.
Влияние на способность управлять транспортными средствами, механизмами. На фоне приема препарата отмечалось возникновение обмороков и головокружения, которые могут влиять на способность управления транспортными средствами или другими механизмами (см. «Побочные действия»). Пациенты, у которых возникают подобные нежелательные реакции, не должны управлять транспортными средствами или другими механизмами.
Форма выпуска
Таблетки, покрытые пленочной оболочкой, 2,5 мг. По 10 или 14 таблеток в блистере из Ал/ПП или Ал/ПВХ-ПВДХ. По 1, 2, 4, 7, 12, 14 блистеров по 14 таблеток или 10 блистеров по 10 таблеток вместе с инструкцией по применению помещены в картонную пачку с контролем первого вскрытия.
Производитель
Наименование и адрес юридического лица,на имя которого выдано регистрационное удостоверение: Байер АГ, Кайзер-Вильгельм-Аллее, 1, 51373 Леверкузен, Германия/Bayer AG, Kaiser-Wilhelm-Allee, 1, 51373 Leverkusen, Germany.
Производство готовой лекарственной формы: Байер АГ, Кайзер-Вильгельм-Аллее, 51368 Леверкузен, Германия/Bayer AG, Kaiser-Wilhelm-Allee, 51368 Leverkusen, Germany.
Вторичная/потребительская упаковка: Байер АГ, Кайзер-Вильгельм-Аллее, 51368 Леверкузен, Германия/Bayer AG, Kaiser-Wilhelm-Allee, 51368 Leverkusen, Germany или Штегеманн Лонферпакунг унд Логистишер Сервис е.К., Уп’н Ниен-Эш 14, Гревен, 48268, Германия/Stegemann Lohnverpackung&Logistischer Service e.K., Up’n Nien Esch 14, 48268 Greven, Germany.
Выпускающий контроль качества: Байер АГ, Кайзер-Вильгельм-Аллее, 51368 Леверкузен, Германия/Bayer AG, Kaiser-Wilhelm-Allee, 51368 Leverkusen, Germany.
Организация, принимающая претензии потребителей: АО «БАЙЕР», 107113, Москва, 3-я Рыбинская ул., 18, стр. 2.
Тел.: +7 (495) 231-12-00.
www.bayer.ru
Условия отпуска из аптек
По рецепту.
Условия хранения
При температуре не выше 30 °C.
Хранить в недоступном для детей месте.
Срок годности
3 года.
Не применять по истечении срока годности, указанного на упаковке.
Описание проверено
-
Крылов Юрий Федорович
(фармаколог, доктор медицинских наук, профессор, академик Международной академии информатизации)
Опыт работы: более 34 лет
Представленная информация о ценах на препараты не является предложением о продаже или покупке товара.
Информация предназначена исключительно для сравнения цен в стационарных аптеках, осуществляющих деятельность в
соответствии со статьей 55 Федерального закона «Об обращении лекарственных средств» от 12.04.2010 № 61-ФЗ.
